
Autoria: Alberto Federman Neto, AFNTECH.
Atualizado e ampliado em 13 de Agosto de 2020.
Neste Terceiro Artigo, veremos alguns Químicos famosos e seu trabalho. Veja também a Primeira e a Segunda partes da Série.
1. ROBERT BOYLE:
O Filósofo Natural e Químico Irlandês, Robert Boyle. Um exemplo de um Químico, que transitou entre a Alquimia e a Química. Um dos primeiros Químicos, ao mesmo tempo o último Alquimista.
Por ser um homem influenciado pelos que o precederam, apesar de ser futurista, Boyle, além de ser um Químico moderno, gostava e estudou e praticou muita Alquimia . Livro, meu exemplar: FARIAS, R.F. “História da Alquimia.” Editora Átomo, Gráfica Bartira, São Paulo, S.P., 2a ed., Pág 77 (2010).
Estudou a transmutação. Link 127. São dele os procedimentos alquímicos tentativos de mudar a natureza de grande massa de metais não nobres, como cobre ou chumbo, através de uso de pequenas quantidades de prata e ouro puros. Veja: OLIVEIRA, A.J. Princípios, Rev. Fil. 22, 39 (2015).
Tratei desse assunto, neste Artigo, e Neste. Veja ainda no texto, o tópico Azoth. Entretanto, Boyle rejeitava a interligação da Alquimia com a Magia. A despia de toda e qualquer aura mágica.Tinha uma visão científica.
Influenciado pelo método científico e pela obra, “Novum Organum” de Francis Bacon, vê muito valor na experimentação, e detalha muito seus experimentos, do ponto de vista qualitativo e quantitativo. Todas as Teorias precisam ser testadas.
É considerado um dos fundadores da Química moderna, “Pai da Química“, e rejeitava mesmo as palavras “Alquimia” e “Alquimista”, substituindo-as pelos termos “Química e Químico” (que haviam sido inventados por Becher).
Fez muitas descobertas simples, mas importantes. Exemplo, usou xarope de violetas de Parma como indicador para bases ou ácidos, além do tornassol, embora o tornassol já fosse conhecido desde os ano 1300 (Arnaud de Villeneuve).
Embora o termômetro tenha sido inventado pelos Italianos Galileo Galilei e Evangelista Torriceli, Boyle usou os primeiros termômetros de álcool. Derivados do termômetro do Duque Ferdinando II da Toscana. POWERS, J.C. Osiris, 29, 158 (2014).
O termômetro de mercúrio foi inventado pelo Pomerânio (hoje é onde fica o Polônia) Daniel Gabriel Fahrenheit. Do qual derivam os termômetros de mercúrio atuais, que nós, os Químicos usamos.
Influenciado por Isaac Newton (Teoria Corpuscular da Luz) e por Epicuro, Boyle adota o “Corpuscularismo“, uma modificação do Atomismo, de Demócrito e Leucipo. Veja este meu outro Artigo. Ele ataca a Teoria dos 4 Elementos e a “Trina Prima” de Paracelso,
Os corpos químicos são compostos por partículas, tipo os átomos, mas que se movimentam continuamente, como se tivessem molas, elasticidade, e tem espaços entre eles, e isso determina suas propriedades. Link 1. Os fenômenos e reações são resultantes de colisões entre essas partículas…Elementos químicos simples não podem ser decompostos.
Note que é já uma noção próxima da visão moderna de átomo. E das moléculas e reações. GAVEZZOTTI, A. CrystEngCom (2013).
As obras mais importantes de Boyle e suas descobertas.
O livro “The Sceptical Chymist.” (1661) onde descreve sua ideias sobre as partículas que compõe a matéria, e propõe uma visão científica e prática, não alquímica, para a Química. Edição de 1661.; Edição de 1911. Outro Link. Edição de 1964. Diversas edições. Edição no projeto Gutenberg; DAVIDSON, J.S “Annotations to Boyle Sceptical Chymist.” (2001). PRINCIPE, L. Nature 469, 30 (2011).
Boyle faz experimentos (Link 13) com a bomba de vácuo de Gasparis Schotti modificada por Otto Von Guericke, e descobre (junto com Link, 18, o Filósofo Natural Inglês Robert Hooke) algo importante: Que a combustão, queima, não pode ocorrer no vácuo, na ausência de ar.
Embora contemporâneo de Stahl, Ele não é ainda um flogista. Pois as publicações de Stahl são uns 30 anos posteriores aos experimentos iniciais de Boyle. Mas os experimentos demonstraram que o ar tinha um papel importante na combustão.
Boyle não rechaça, nem comenta sobre o Flogisto, mas fala que os corpúsculos, partículas de enxofre, ou de fogo, podem compor a matéria…. Links: 3, 4, 5. Link 6. 7, 8, 9, 10, 11, 12,
Mas usando os experimentos de Boyle, quase cem anos depois, em 1753, o Químico Russo Mikhail Vasilyevich Lomonosov mostraria que o Flogisto não existia.
Esses experimentos e pesquisas de Boyle com o ar e os gases, publicados a partir do Livro: “New Experiments Physico-Mechanical, Touching the Spring of the Air, and It’s Effects.” (1660), Link 14, 15, Edição de 1682, 1669, Link 17, 19, 20, 21, 22. Edição em Yale, BOYLE, R. “A Defence of the Doctrine Touching the Spring and Weight of the Air, ” Editor. ROBINSON, T. (1662).
seriam muito importantes e culminariam nos resultados conhecidos como as “Leis dos Gases“. depois reestudadas e modificadas pelo Químico Francês Edme Mariotte, em 1676. MARIOTTE, E. “Second Essai de la Nature de L’Air.” (1676). VANDER, P. “Ouvres de Monsieur Mariotte.” (1717). Link 31.
Para Boyle, o ar era um fluido composto de partículas que se movimentavam e elásticas, como se tivessem molas. “The Boyle Papers. “, vol 9.
Lei de Boyle-Mariotte, tão importante em Química e constante em todos os livros texto. Links: 23, 24, 25, 26, 27, 28, 29, 30
2. JOHN DALTON:
Físico e Químico Inglês. John Dalton. Link 31.
Ele retoma a ideia de Boyle, de que os átomos compõe a matéria, mas a sistematiza para compor todas as moléculas, em uma “Filosofia Química”. Para ele, os átomos, como em Demócrito, são indivisíveis.“Manual Rosacruz.” Edição Espanhola. Link 46. Livro, exemplar do Autor deste Artigo: SPENCER LEWIS, H. “Manual Rosacruz.” Editora AMORC (1980). O Autor deste Blog é membro da Ordem Rosacruz, desde 1975.
A partir de 1808. DALTON, J. “A new System of Chemical Philosophy.” (1808-1827), Links: 31, 32, 33, 34, 35, 36, 37, 38, 39, 40. Links 41, 42, 43, 44, 45. Edição de 1964.
Esse trabalho é a base da moderna Teoria Atômica. O Atomismo. Voltaremos a falar disso em outro futuro artigo. GONZÀLEZ, I.P. “El Atomismo en Química.”, Universidade de Alicante, Espanha. (2012).
Como Boyle, Dalton também estudou os gases. é dele a “Lei das Pressões Parciais“, “Lei de Dalton” HELMSTINE, T. (2019). DALTON, J. “Memoirs of the Literary and Philosophical Society of Manchester”, 5, 595 (1802). Obras de Dalton. Link 87, 88.
3. KARL SCHEELE:
Químico e Farmacêutico Sueco Karl Wilhelm Scheele.
Contemporâneo de Lavoisier, mas em contraste com ele, Scheele é um Flogista.
Era um experimentalista brilhante , link 106, e observou e descobriu muitos elementos químicos e substâncias, embora não tenha publicado oficialmente tudo.
Teria descoberto o manganês, molibdênio, tungstênio, bário, o hidrogênio, os nitritos, arsenito de cobre (Verde de Scheele) os ácidos tartárico, oxálico, cítrico, lático, úrico, fluorídrico, cianídrico, ácido arsenioso, gálico, benzóico, glicerol, gás sulfídrico, tetrafluoreto de silício, lactose, etc…. Link 51. Link 67. Preparou puros o ácido clorídrico e o gás clorídrico.
Tentava repetir os experimentos de Lavoisier, com o intuito de comprovar o Flogisto. Aquecendo o óxido de mercúrio, ou sais oxigenados, ou alguns nitratos, isolou seu “Ar de Fogo” ou “Ar Combustível“, que era na realidade o Oxigênio de Lavoisier e Priestley.
Teria descoberto o Oxigênio em 1772, mesmo em 1771, portanto dois anos antes de Lavoisier e Priestley (descobridor oficial) Links: 46, 47, 48, 49, 50, 51, 52, 53, 54, 55. Links 56, 57, 58. “Ar Deflogisticado ” de PRIESTLEY, J. Phil Trans. 65, 384, 1775. Link 73. Link 81.
Mas só o publicaria em 1777, na sua principal Obra, Chemische Abhandlung von der Luft und dem Feuer.” Tradução Livre do Título: “Tratado Químico sobre o Ar e do Fogo.” Edição de 1894. Link 59. Link 60. Link 61. 62, 63, 64, 65, 66. Link 67. Tradução para o Francês de DIETRICH (1781). Tradução em Inglês, de 1780. 1781. Link 72. Link 74, 75 , 102. Link 85. 105,
Alguns Historiadores, porém dizem que Scheele havia publicado em 1771, seu “Ar de Fogo”, em artigos em revistas pequenas e pouco conhecidas, e por isso, sua descoberta ficou ignorada, mas teria sido o verdadeiro descobridor. Link 86. 87. 88. 89. 90 ,91, Link 103. Há indicações de que Scheele havia escrito a Lavoisier e Priestley, informando que a descoberta do seu “Ar de Fogo” era anterior, mas foi ignorado! 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 104, 106, 107 .
Scheele também descobriu o halogênio cloro. Tratando um mineral de manganês, a Pirolusita (bióxido de manganês), que descobrira, com ácido clorídrico aquoso, pela primeira vez, prepara o cloro, o halogênio cloro, um gás verde venenoso. Por isso, ele também é o verdadeiro descobridor da oxidação. Antes de Lavoisier. Ele chamou o cloro de “Espírito de Sal Deflogisticado“ ou “Ácido Marinho Deflogisticado“. SCHEELE, K.W. Proc. Roy. Scient. Acad. Sweden, 89 e 177 (1774). Veja a referência 6, deste Link. e Este.
Scheele ainda pensava que seu elemento contivesse oxigênio, fosse um ácido oxigenado, Lavoisier também… Mas em 1810, Humphy Davy mostraria que o cloro era um elemento simples.
Dissolvendo o cloro gás em água, ou em lixívia alcalina de soda ou potassa, ou tratando a cal com cloro, Scheele descobre: a água de cloro (uma mistura de ácidos clorídrico e hipocloroso) :
H2O + Cl2 = HCl + HClO
É a base do método moderno de clorar a água para desinfetá-la. (1894).
Eu usei água de cloro como reagente para obter outros halogênios, a partir de brometos e iodetos (FEDERMAN NETO, Curso Técnico em Química Industrial, Liceu Eduardo Prado, São Paulo, S.P. (1971) ).
Embora água de cloro possa ser feita, mais fácil a partir de hipocloritos, Link 89, do que de dióxido de manganês e ácido clorídrico (link 90, 91), HOLMES Jr., R.H. 74, 1326 (1997). seu uso em análise química é técnica obsoleta e muito em desuso.
Borbulhando o cloro em lixívias de soda ou potassa, Scheele obteve os hipocloritos de sódio, potássio e cálcio. NaClO, KClO e Ca(ClO)2. É a água sanitária, “Água de Lavadeira“! ROSCOE, E. “A Treatise on Chemistry.” (1911). Link 80. É o cloro de piscina, e o HTH.
Scheele conseguiu mostrar que o ar é uma mistura de gases, Curiosamente, ao tentar restaurar a Teoria do Flogisto, o trabalho de Scheele contribuiu para acabar com ele de vez! Sem o “Ar de Fogo”, não podia mais ocorrer combustão. Links 68, 69, 70, 71. Link 75, 76, 77, 78, 79, 80.
Em Scheele, também encontramos uma das primeiras tentativas de uniformizar a nomenclatura e o jargão químico. Eis os símbolos que ele propõe para representar os corpos químicos e os elementos. Uppsala, Suécia, (1775). Link 82. 83 .
4. JOSEPH PRIESTLEY E JOSEPH BLACK:
Químico e Filósofo Natural Inglês, 1733 a 1804. Como Scheele e muitos Químicos contemporâneos dele, Priestley é um Flogista. Grande número de trabalhos dele, defendem o Flogisto!
Por volta de 1700, ainda o ar podia ser considerado como se fosse um elemento químico simples e constituinte da matéria.
Apesar disso, observando e analisando e modificando os experimentos de Robert Boyle (Item 1) , o Químico Inglês John Mayow havia demonstrado (1674) que o ar é uma mistura que contém uma parte “ativa” respirável e uma parte, “inativa” inerte. Link 107. 108. 109. 110. MARROW, J. “Tractatus Quinque Medico-Physici.” Traduzido ao Inglês: “Medico-Physical Works.” (1674).
Em 1754-1755, o Químico Escocês Joseph Black prepara o gás carbônico a partir do aquecimento da cal, ( chamou-o “Air Fixo“) Link 118, e descobre que ele existe no ar, não sustenta a Vida, mas está envolvido na respiração. Trabalhos de Joseph Black, Links 121, 122.123. 124.125. 126.
Mas Black não associou o seu gás, do qual é oficialmente o descobridor, Link 120, ao obtido pelo Filósofo Natural e Alquimista Belga Jean Baptiste Van Helmont, preparado pela queima do carvão. Link 111 , 112 , 113, 114, 115, chamado “Espírito Silvestre”(1640). Também Scheele havia preparado o gás carbônico.
As obras de Van Helmont (“Ortus Medicinae, Vel Opera et Opuscula Omnia“) foram coletadas e publicadas em 1648, por seu Filho, o Alquimista Belga Franciscus Mercurius Van Helmont. Depois republicadas pelo neto dele. Links 116, 117.
Recapitulando, então já era sabido que o ar podia ser uma mistura de gases. Em 1772, Priestley estudava os gases do ar, dentre eles o “Ar Fixo” de Black: PRIESTLEY, J. “Observations on Different Kinds of Air.” Phil. Trans. 62, 147 (1772). Reportou os 3 três tipos de ar: “Ar Fixo” (hoje, gás carbônico), “Ar Inflamável” (hoje, hidrogênio) e “Ar Mefítico”, uma porção que restava após uma queima e que não podia mais alimentar a combustão.
Continuou estudando uma série de gases, sempre interpretando suas descobertas em termos de Flogisto. Exemplos, quando calcinava “Cales” carbonadas (hoje seriam carbonatos) claro, obtinha gás carbônico,”Ar Fixo” de Black…
Elaborou experimentos que ficaram famosos. Links: 128, 129, 130, 132. Encerrou uma vela acesa em uma campânula. a chama se extinguia porque ela havia saturado o ar com o Flogisto, que não podia mais ser absorvido, a campânula agora conteria “Ar Fixo” e “Ar Mefítico”. Explicação real. A vela consumiu o oxigênio….
Então ele colocou dentro da campânula, uma planta…Colocando um rato agora na campânula, o rato respirava, não morria (oxigênio gerado pela planta). Para Priestley, a planta capturava Flogisto do ar, dando “força” ao ar tornando-o novamente respirável…
A idéia dele era “isolar” o Flogisto. Recapitulemos. Para os Flogistas, os metais eram combinações de uma “cal” e Flogisto… Priestley tomou o óxido vermelho de mercúrio (“cal do mercúrio”) e o aqueceu, usando raios solares condensados por uma lente. Claro, formou-se o metal o oxigênio mas para Priestley , o metal se formou da cal e Flogisto.
Equação, moderna:
2 HgO = 2 Hg + O2
E recolheu um gás, que fortemente alimentava a combustão de maneira intensa, e era muito respirável…, “Ar Respirável”, melhorado. O chamou “Ar Deflogisticado“. Era o Oxigênio, mas Priestley acreditava ter detectado o Flogisto.
Em 1775, publica seus experimentos novos um Artigo: PRIESTLEY, J. “An Account of Further Discoveries in Air.” Phil. Trans. 65, 384 (1775).
O próprio Priestley coletou todos os seus trabalhos sobre os gases, em seis volumes, entre 1772 e 1790. “Experiments and Observations of Different Kinds of Air.” Volumes 2 e 3, Volume 1, Volume 2. Outro Link do Volume 2. Completo, republicado em 3 Volumes. Links: 134, 135.
Curiosamente, Priestley defendeu o Flogisto até o fim de sua vida, e publicou um artigo, no qual afirma ter convertido água em ar. PRIESTLEY, J. Phil. Trans. Roy Soc. London 73, 398 (1783).
Em que pese ser um Flogista convicto, o trabalho de Priestley é fenomenal. Ele reporta o oxigênio (descoberta atríbuída a ele, mas como vimos, é de Scheele), mas descobre a fotossíntese, os mecanismos da respiração e descobriu e isolou dezenas de gases novos. Links: 136, 137, 138.
5. HENRY CAVENDISH E DANIEL RUTHERFORD:
Como muitos Químicos da época,Também são Flogistas.
Henry Cavendish. Químico, Francês de nascimento, (Nice, que pertencia, na época, ao reino da Sardenha) mas de nacionalidade Inglesa.
A ele se credita a descoberta do Hidrogênio, “Ar Inflamável”. “The Scientific Papers of Henry Cavendish.” (1921). Link 139. 140. Em 1766. CAVENDISH, H. “Experiments on Air.” Phil. Trans. 75, 372 (1766), republicado em (1785). CAVENDISH, H. “Three Papers on Factitious Air.” Phil. Trans. 56, 141 (1766). Link 152.
O Hidrogênio havia sido observado antes, por Paracelso, por Boyle e por Scheele, mas foi Cavendish que o estudou em detalhes e mediu a sua densidade e propriedades, e o confundiu com o hipotético Flogisto.
Alguns atribuem a descoberta do Nitrogênio Link 141, a Cavendish e a Scheele, ou a Priestley, pois o haviam obtido, por volta de 1760, a partir do ar, após consumir todo o oxigênio, por queima, ou com carvão aquecido. Era o resíduo do chamado “Ar Mefítico” de Priestley e do “Ar Fixo” de Black. O chamaram “Ar Flogisticado”.
Mas eles pouco conheciam sobre a verdadeira Natureza do Nitrogênio, que foi preparado, perfeitamente caracterizado , pelo Médico, Químico e Físico Escocês Daniel Rutherford. 1772. Ele foi aluno de Joseph Black.
RUTHERFORD, D. “Dissertatio Inaugularis di Aere Fixo Dicto aut Mephitico.” Tese de Doutorado em Medicina, Universidade de Edimburgo, Escócia (1772). Tradução Livre do Título: “Dissertação Inaugural do Ar Fixo, Isto é do Chamado Ar Mefítico.” DOBBIN, N. J. Chem Educ. 12, 370 (1935). WEEKS, M.E J. Chem, Educ.11, 101 (1934).
Rutherford reconheceu o nitrogênio como substância simples, mas não como elemento químico. Foi também Rutherford quem diferenciou o “Ar Mefítico”, Nitrogênio, do “Ar Fixo”, Gás Carbônico.
Cavendish também estabeleceu com exatidão, a composição química do ar e da água. CAVENDISH, H. “Experiments on Air” Phil. Trans. 75, 372 (1785). CAVENDISH, H. Phil. Trans. 74, 119 (1784). Link 142. Link 143. Link 144. 145, 146, 147, 148, 149, 150, 151. “Three Philosophers: Lavoisier, Priestley and Cavendish.” Ann. Intern. Med, 9, 1940 (1936).
6. LAVOISIER E OUTROS:
Antoine Laurent Lavoisier, Químico Francês. 1743 a 1794. Links 153, 154.
Considerado Criador da Química Moderna, Autor de uma chamada “Revolução Química” pois faz muitos experimentos, que irão derrubar a Teoria do Flogisto. Além de modernizar a nomenclatura e a linguagem química. A esposa de Lavoisier, Química autodidata, atacaria o Flogisto com ainda mais veemência que o marido.
Ele mostrou que os metais se combinam com o Oxigênio para formar óxidos. A oxidação não era decomposição e sim uma reação de combinação. Não havia a “Perda de Flogisto“.
Seus experimentos, são rigorosamente exatos, devido ao uso de balanças extremamente precisas. Ele consegue medir a quantidade de Oxigênio do ar consumida, e estabelece o papel do oxigênio na combustão (“Teoria da Combustão” ,”Teoria da Oxidação“). Que terminará por substituir o Flogisto.
Além disso, descobre que a massa dos produtos de uma reação é igual a massa dos reagentes. “Lei da Conservação da Massa”.
Apesar disso, parte do seu trabalho pode ser envolvido em certa controvérsia, pois não teria sido o descobridor da oxidação (e sim Scheele, ao tratar a Pirolusita pelo ácido clorídrico). GUERLAC, H. “Lavoisier – The Crucial Year. The Background and Origin of His First Experiments on Combustions, in 1772.” Cornell University Press. Ithaca, NY, EUA (1961).
Mesmo os trabalhos que resultaram na conservação da massa, oxigenio, combustão e ar, eram baseados (ele, Lavoisier, mesmo cita os experimentos de outros) que já haviam sido feitos anteriormente, apesar de forma preliminar, por Cavendish , Priestley e por Joseph Black .Link 166.
Semelhantemente, enunciar a “Lei da Conservação da Massa” e refutar o Flogisto, teria sido feito pelo Químico Russo Mikhail Vasilyevich Lomonosov, 14 anos antes de Lavoisier. POMPER, P. Ambix, 10, 119 (1962). SHILTSEV, V. (Tradutor) (2018) LOMONOSOV, M. “Meditationes de Solido et Fluido.” “Reflections on the Solidity and Fluidity of Bodies” (1760). Link 155, 156, 157. Link 158. Não se sabe ao certo se Lavoisier conhecia o trabalho de Lomonosov, mas certos Autores dizem que sim… LEICESTER, H.M. Isis, 58, 240 (1967).
Mas Lavoisier tem grande mérito. Suas descobertas são precisas e exatas e culminarão com a descoberta do verdadeiro mecanismo da combustão e da oxidação.
Fez grande número de experimentos. Exemplos, estudou a combustão, a queima do enxôfre, do fósforo, dos metais, madeiras, gases combustíveis etc… e chegou a conclusão de que fósforo e enxôfre eram elementos simples. Reconhece também o nitrogênio como elemento simples. LAVOISIER, M. Hist. Acad. Roy. Scienc. 416 (1783). Ibid. 563 . Também confirma a composição química da água e descobre que ela é um óxido. Link 164.
Pelo fato do enxôfre, do fósforo, do bórax etc… ao queimarem, formarem o que se chama hoje “óxidos ácidos”, Lavoisier pensava que todos os ácidos continham oxigênio. Links 166, e por isso, batizou o “‘Ar Deflogisticado” de Priestley, OXIGÊNIO. “Gerador de Ácidos”
Aqui mais um pouco de polêmica, pois vimos que Lavoisier, ao contrário do que dizia, não descobriu o oxigênio. Foi Scheele e Priestly. Aliás, não descobriu nem o Oxigênio (Scheele), nem o Hidrogênio (Cavendish), nem o Nitrogênio (Rutherford) e nem o Gás Carbônico (Black).
Mas o trabalho de Lavoisier, rompe com a Alquimia, e lança as bases do conceito de “Elemento Químico”.Link 184.
Em 1786, Lavoisier publica seu Trabalho (de 1777) , “Réflexions sur le phlogistique, Pour Servir de Suite à la Théorie de la Combustion et de la Calcination.” BEST, N.W. Found. Chem. 17, 137 (2015). LAVOISIER, M. Hist. Acad. Roy. Scienc. 505 (1786).
Nesse trabalho, refuta o Flogisto, mas sugere um “Fluido”, o Calórico, Link 159, 160, 161, 162 , 163. sem massa, mas que flui do corpo mais frio ao mais quente, e pode ser incorporado pelo corpo, ou substância, aumentando o peso. Para Lavoisier, o Calórico é um Elemento Químico, e a Luz, também:
Citação: LAVOISIER, A.L. Hist. Acad. Roy. Scienc. 505 (1786), Pág 514:
La matière de la chaleur & de la lumière ayant la propriété de pénétrer, de paner à travers les vaiueaux, il iunit, pour revivifier ces chaux, de les exposer à un certain degré de chaleur, & de les garantir du contact de l’air.
Tradução Livre: A matéria do calor e da luz, tendo a propriedade de penetrar através dos vasos de reação, se unifica para revivificar as cales, expo-las a um certo grau de calor e lhes garantir um contacto com o ar.
Citação LAVOISIER, A.L. “Traité Elementaire de Chemie.” (1793). Pág. 200:
Le Calorique se fixe dans le corps, de manière même a constituer les parties solides.
Tradução Livre: O Calórico se fixa ao corpo (composto), de maneira mesmo a constituir suas partes sólidas.
“Lavoisier and The Caloric Theory.”. LAVOISIER, A. L. “De la Combination de las Matiére du Feu Avec des Fluides Évaporables.” Hist. Acad. Roy. Scienc. 420 (1777).
Depois da Morte de Lavoisier, seria encontrado um trabalho atribuído a ele, “Mémoire sur Le Feu Élémentaire.” onde novamente descreve o Calórico como componente da matéria. GUERLAC, H. Isis, 125 (1959).
Não consegui achar a referência original dessa memória, 1772, Ela não consta na Revista da Academie Royale de Sciences. Google Academic:
[CITAÇÃO] Memoire sur le feu elementaire
AL Lavoisier – 1772 – Memoire de l’Academie Royale des …
mas o fato é que o Fogo Elementar é citado neste Livro, escrito em Francês pelo Químico de Portugal (Químico, Físico e Filósofo Natural João Jacinto de Magalhães , Links 188, 189, 190, 191, 192, 193) (outros livros de Autoria dele), descendente de franceses, Jean Hyacinthe de Magellan: MAGELLAN, J.H “Essai sur la Nouvelle Theorie du Feu Élémentaire et de la Chaleur des Corps.” Tradução Livre do Título: “Ensaio Sobre a Nova Teoria do Fogo Elementar e do Calor dos Corpos.” Pág 167 (1780) .
Note que o Calórico de Lavoisier vai de encontro da “Teoria do Calor Latente” de Joseph Black (descobridor do Calor Específico), mas para este, o calor é uma energia. Tanto que é Flogista. Assim como o calor era uma energia para Scheele. Que faz distinção entre o calor radiante e calor de condução ou convecção.
BEST, N.W Found. Chem. 18, 3 (2016). Link 171. Tradução dos Artigos de LAVOISIER, A.L. “Reflexions sur le Phlogiston.” Partes I e II.
Note que Lavoisier adota e modifica o “Calórico” de Joseph Black [ ROBINSON, J. (Editor) BLACK, J. “Lectures on the Elements of Chemistry.” edição de (1803) ] para considerá-lo um “Elemento Químico” componente da matéria. DAUMAS, M. ; COLIN, A. (Editor) Thalès 6, 69 (1949-1950).
Mas não usa a palavra “Calórico”, irá faze-lo após o Químico Francês Louis Bernard Guyton de Morveau, em uma Memória publicada por vários Autores: “Mémoire sur le Développement des Principes de la Nomenclature Méthodique.“, publicada na Obra: MORVEAU, L.B.G; LAVOISIER, A.L.; BERTHOLLET, C.L; FOURCROY, A.F. “Methode de la Nomenclature Chimique.” Cuchet Librairie, Paris, França (1787). Edição de 1787. Outros coautores seriam os Químicos Franceses Claude Louis Berthollet, e Antoine François De Fourcroy.
Junto do Matemático e Físico Francês Pierre Simon Laplace, Lavoisier estudaria mais o Calórico. Link 167. Link 168. 170. Para eles o Calórico era um Fluido em movimento e composto de partículas, como se fosse um Elemento Químico.LAVOISIER, A.L. “Memoires de Chemie.” Vol. 1 e Vol. 2. Republicadas em (1803). LAVOISIER, M.; DE LA PLACE, “Memoire su La Chaleur.“ Hist. Acad. Roy Cienc. 355 (1780). MORRIS, R.J. Brit. J. Hist. Scienc. 6, 1 (1972).
Embora errada, a Teoria do Calórico, lançou as bases da Calorimetria e da Termodinâmica. LAVOISIER, A. “Memoire Sur da Chaleur.” Edição de (1892). TAVARES, G.W.; PRADO, A.G.S. Quím Nova, 33, 1987 (2010). CHAGAS, A.P. Quím Nova, 15, 269 (1992). Hist. Ciênc. Ens. 18, (2018). Link 185.
A Hipótese do Calórico de Lavoisier sobreviveria até por volta de 1890. SMEATON, W.A. Bull. Hist. Chem. 5, 4 (1989). Seria derrubada pelo Químico Francês Marcellin Pierre Eugène Berthelot. DONOVAN, A. Osiris, 4, 214 (1988). BERTHELOT, M. Revue de Deux Mondes, 98, 347 (1890).
As obras de Lavoisier, principalmente “Traité Elementaire de Chemie.” (1789). Link 172 Note a assinatura do texto. A edição que foi digitalizada pertenceu a Moseley, um químico famoso, um dos pioneiros da Teoria Atômica. Henry Gwyn Jeffreys Moseley.
173, 174, 175, 176, Edição de 1793. Edição de 1789. Link 177, 178, Link 180. Traduções para Inglês, dessa e de diversas obras importantes em Química. Link do primeiro volume. Link do segundo volume. Link do Site “Domínio Público”. Digitalização Moderna, feita da edição de 1789.
São um marco da Revolução Química Link 183. 185, (depois viriam melhoramentos da tecnologia) e da nomenclatura química moderna. Exemplo, pela primeira vez usam a expressão “radical”, para designar íons ou grupos funcionais. LAFONT, O. Rev. Hist. Pharm. 352, 447 (2006). Também ele denomina e classifica vários ácidos, bases e sais. Link 181.
Mas em Lavoisier, a defesa do Calórico, como uma substância ou elemento fundamental e incorporável na matéria, é claramente perceptível:
“Méthode de Nomenclature.” Pág. 32:
E laisse aller, de moins en partie, la lumiére e le calorique, que sont les principes constituants comme l’air vital. Il falloit considerer cette substance et la designer dans cet état de plus grande simplicité.
Tradução Livre: E deixa ir, pelo menos em parte, a luz e o calórico, que são os princípios constituintes do ar vital. Façamos considerar essa substância, e a designá-la nesse estado de maior simplicidade.
Encore faut-il observé q’ont n’obtient point l’azote seul e isolé mais combiné avec le calorique.
Tradução Livre: Agora façamos observar que não obtivemos pontualmente o azoto (nitrogênio) sózinho e isolado, mas combinado com o calórico.
No mesmo livro, os autores tabelam o calórico e a luz, várias vezes, como elementos químicos. Págs. 42, 45, 56 etc…
Uma parte muito importante do trabalho de Lavoisier, é porque foi um dos primeiros, junto com Morveau, Fourcroy e Berthollet, a procurar uniformizar, sistematizar e modernizar a nomenclatura química, afastando-a do complicado jargão da Alquimia.
O Brasileiro José Bonifácio de Andrada e Silva estudaria Química na França com Fourcroy, e depois lecionaria, mas claramente era Flogista. LIBERALLI, C.H. Rev. Hist. 45, 367 (1972). Link 200. Link 201. FILGUEIRAS, C.A.L. Quim. Nova 9, 263 (1986).
Lavoisier ainda usa símbolos semelhantes aos da Alquimia:
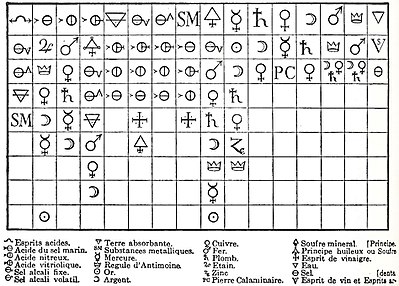
Mas já propõe uma Nomenclatura moderna para as substâncias e os Elementos Químicos. Mas note que cita a Luz e o “Calórico”, como Elementos Químicos:

Lavoisier confirmou a composição do ar (Cavendish) (Link 182) e da água (Priestley) (link 181). Descobre que o Oxigênio, o Hidrogênio, o Fósforo, o Enxôfre e o Nitrogênio são Elementos Químicos, mas para ele, os metais não são elementos simples. BUSTAMANTE, J.A.P. ILUIL, 25, 29 (2002).
E todos os ácidos precisavam conter oxigênio, o que se sabe hoje é um erro.
Oficialmente, com Lavoisier se encerra a Alquimia. Após ele, é a Química Moderna.
Mas na minha opinião, a Alquimia vai terminando após Becher e Stahl, e até um pouco antes disso, com Boyle. Outros Autores tem a mesma opinião. Link 179, 180. 181, 182. TOSI, L. Quim. Nova 12, 33 (1989) . MOCELLIN, R.C.; DUTRA, L.H. “Lavoisier e a Longa Revolução na Química.” Dissertação de Mestrado, Centro de Filosofia e Ciências Humanas, Universidade Federal de Santa Catarina, Florianópolis, S.C. .
Isso porque o Flogisto teve seus méritos. Era uma Teoria Científica e bem elaborada. Foi aceita por quase 120 anos.
A noção de alguns Autores, de que o Flogisto atrasou a Química, Links: 183, 184, 185, 186, ao meu ver, é incorreta. Se o Flogisto houvesse atrasado a Química, não teriamos tido as fabulosas descobertas de Priestley, Cavendish, Scheele, e muitos outros Flogistas.
Citando o químico Francês Pierre Josephe Macquer ,contemporâneo de Lavoisier. MACQUER, P.J “Notes di Cours de Chemie de P.J Macquer” Achados em 1800. Link 187. Suas obras principais são: “Diccionaire de Chemie.“, “Elements de Chemie. Teorique e Practique.” Existem muitas traduções e edições.
Junto com Lavoisier, Macquer é o primeiro a conseguir fundir a platina. Links: 204, 205. MORIN, C. “La Platine, L’Or Blanc.” (1758). Link 206. McDONALD, D.; HUNT, L.B. “A History of Platinum and its Allied Metals.” Editora Johnson Matthey. (1982).
Macquer é um herdeiro da tradição “semi Alquimíca” de Isaac Newton. Para ele, o Flogisto é um elemento que existe na luz e no calor. LECAILLE, C. Ciencias, 034 (1994). Link 188. Ele tenta árduamente reconciliar o Flogisto com as Teorias Antiflogistas de Lavoisier. WISNIAK, J. Educ. Quim. 15, 300 (2004). GILMAS, O.G. Sobre el “Discours sur le phlogistique et sur plusieurs points importants de Chymie.”, 1774.” Actas del III Congreso de la Sociedad Española de Historia de las Ciencias (1986). LEWOWICZ, L. Monografia. “The Purloined Referent: Lavoisier and the Disappearance of Phlogiston.” (2009). DE BERG, K.C. Scienc. Educ. 17, 265 (2008). DUVEEN, D.I.; KLICKSTEIN, Osiris, 12, 342 (1956).
Outro Químico a tentar reconciliar os pensamentos de Lavoisier ao Flogisto, é Guyton de Morveau. MOCELLIN, R.C Int. J. Hist. Cienc. 10, 22 (2011). Morveau de início é um Flogista, depois adota as teoria de Lavoisier. DUVEEN, D.I., et al.,Loc. Cit. De fato, passará a Vida tentando conciliar as duas teorias. MOCELLIN, R.C, Loc. Cit. . MOCELLIN, R.C. . BENSAUDE-VINCENT, B (Orientadora) “Louis Bernard Guython de Morveau, Chimiste e Professeur au Siecle des Lumieres.” Tese de Doutorado em História das Ciência, Universidade Paris Quest, Nanterre, França (2009). Link 203.
Certos Autores dizem, era possível conciliar o Flogisto com as Teorias de Lavoisier, ao menos qualitativamente. SCOTT, J.H. J. Chem. Educ. 29, 360 (1952).
Citamos Macquer aqui, porque ele também contribuiu no estabelecimento da nova nomenclatura em Química. a Revolução Química. SMEATON, W.A. Ann. Scienc. 10, 87 (1954). Escreve o primeiro Dicionário de Química. NEVILLE, R.G. J. Chem. Educ. 46, 486 (1966). MACQUER, P.J. “Dictionnaire de Chemie.” 2 Ed., Vol 2 (1778).
Embora os estudos de Lavoisier tendo refutado o Flogisto, muitos Químicos, mesmo do século XIX, ainda eram Flogistas. ALLCHIN, D. Ambix, 39, 110 (1992). GONÇALVES, P.W. Ciênc. Educ. 14, 519 (2008). CHANG, Centaurus, 51, 239 (2009). WISNIAK, J. Indian J. Chem Tech. 11, 732 (2004). HOLMES, F.L. Nuova Voltiana 2, 73 (2000). MAUSKOP, S. Ambix, 49, 185 (2002). LE COZE, J. Compt. Rend. Chim. 11, 772 (2008).
7. BERZELIUS:
Depois de Lavoisier ter abandonado a nomenclatura e os símbolos alquímicos, foi Berzelius um modernizador, um continuador dessa “Revolução Química“, já no século XIX.
Jons Jacob Berzelius, (1779-1848), Médico e Químico Sueco. De origem camponêsa e pobre, precisou interromper seus estudos de Medicina, continuando-os depois, no ano seguinte, pois ganhara uma modesta bolsa de estudos.
No decorrer da faculdade, tomou gosto pela Química.
Influenciado pelo Médico e Químico Suiço Christopher Girtanner, do qual lera a obra: GIRTANNER, C.; UNGER, J.F (Editor) “Anfangsgrunde Der Antiphlogistichen Chemie.” Tradução Livre do título; “Fundamentos da Química Antiflogística.” Berlim, Alemanha (1801).
Tornou-se um seguidor da Química Antiflogística de Lavoisier e do conceito, na época relativamente novo, de Elemento Químico, o que lhe traria críticas de seus professores! Alijado de usar o laboratório da Universidade, alugaria um quarto em um porão de uma casa, sem janela, mas com lareira, e lá improvisou um pequeno laboratório! Preparava o ferricianeto de potássio que usava, a partir de um Azul da Prússia impuro e de baixa qualidade, que comprava em um bazar!
Formando-se em Medicina e trabalhando com Química, se tornaria um dos maiores Químicos de seu tempo, descobridor, ou isolador em forma purificada, de até 8 elementos quimicos práticamente novos ou novos; cério (1803), selênio (1817), tório (1828), silício (1823), zircônio (1824), vanádio, lítio e titânio (1825). Outro Link.
Como Lavoisier fizera antes, ele pregava e fez a modificação, internacionalização e sistematização da nomenclatura química, e o abandono dos enigmáticos termos e símbolos alquímicos.
Por exemplo, hoje sabemos que cloreto é Cl-, sulfato é SO4–, fosfato é PO4-3 etc… Quem fez isso? Berzelius… , ele criou a teoria dos “radicais” inorgânicos e orgânicos, hoje, os “grupos funcionais”.
Também, práticamente inventou a Química Analítica, dosou e determinou a fórmula molecular de centenas de compostos e mediu os “pesos atômicos” de dezenas de elementos. Um trabalho muito inovador!
Algumas vezes, os compostos eram diferentes, propriedades diferentes, mas mesma fórmula bruta… São os “isômeros”. Por isso, Berzelius é o descobridor da “Isomeria“.
O trabalho sensacional e muito inovador de Berzelius, irá influenciar muitos outros pioneiros da Química Analítica, famosos, dentre eles: O Alemão Leopold Gmelin, o Francês Jean Baptiste André Dumas, o também Francês Joseph Louis Proust (da “Lei das Proporções Definidas”).
Assim Berzelius foi um pioneiro. Moderniza a Química, cria nova nomenclatura, inventa métodos de análise, isola e determina a fórmula de compostos, mede pesos atômicos e descobre vários elementos químicos novos. BERZELIUS. J. Phil. Mag. 41, 81 (1813). BERZELIUS, J.J Ann. Phys. 53, 393 (1816). PRIDEAUX, J. Phil. Mag. Ann. 8, 161 (1830). MacNEVIN, W.M. J. Chem. Educ. 31, 207 (1954).
Descobre a Catálise, em 1836. MOULIJN, J.A.; VAN LEEUWEN, P.W.N.M.; VAN SANTEN, L.A. Stud. Surf. Scienc. Cat. 79, 3 (1993).
Também dedicou-se à Eletroquímica, eletrólise e ionização, da qual, junto com o Inglês (ou Celta, Cornish) Humphry Davy, e outros, é um dos iniciadores. Link: 16. Berzelius elabora a “Teoria dos Íons“, pela qual todo átomo é eletrificado, os metais e o hidrogênio são positivos e os não metais, são negativos. Espécies elétricamente carregadas. São os íons. cátions e ânions.
Berzelius discordava das “Leis da Eletroquímica” de Michael Faraday (veja abaixo), porque Faraday fazia distinção entre a “força de uma eletricidade” e a quantidade de eletricidade que passava na solução. GURALNICK, S.M. Isis, 70, 59 (1979).
Também não concordava com Faraday acerca da origem comum de todas as energias do Universo, “Teoria do Campo Unificado“. DUMAS, M. Lond. Edin. Dub. Phil. Mag. Scienc. J. 17, 179 (1840). VON REICHENBACH, “Researches on Magnetism Etc…” Editora Taylor, Walton and Maberly, Londres, Inglaterra (1850).
Acreditava sim, em uma “Força Vital” nos compostos orgânicos. BERZELIUS, J. J. Franklin Inst. 5, 331 (1836). Citado por DAVIES, S. (2017). Isso seria derrubado, após a Sintese da Uréia, a partir de um sal inorgânico, por seu amigo, o Químico Alemão Friedrich Wöhler, WOHLER, F. Ann. Phys. Chem. 88, 253 (1828), citado aqui.
Porém Berzelius ainda discordava, achava necessária a Força Vital, embora preconizasse que compostos orgânicos e inorgânicos obedecessem às mesmas leis. BERZELIUS, J.J.; BOYÈ, M.H.; LEAMING, M.D. (Tradutores) “The Kidneys and the Urine.” Editora: Lea & Blanchard, Filadélfia, EUA, Pág 74 (1843).
O trabalho com eletroquímica gerou uma Teoria enunciada por Berzelius, a “Teoria do Dualismo Eletroquímico” pela qual todas as moléculas seriam derivadas de óxidos ácidos e óxidos básicos. ROSE, H.; BERZELIUS, J.J. “Berzelius.” Editora George Reimer, Berlim, Alemanha, Págs 28, 32, 35, 42, 54 (1852).
Ele publicaria essa teoria, em sueco, em um muito famoso Artigo, que alunos dele traduziriam, para o Francês. BERZELIUS, J.J. “Essai Sur La Théorie des Proportions Chimiques et sur L’Influence Chimique de la Électricité.” Editora Méquignon-Marvais, Paris, França (1819).
Como Lavoisier, (oxigênio é o gerador de ácidos) , Berzelius achava que todos os ácidos deveriam conter oxigênio… Nature News, “Jons Jacob Berzelius” Nature, 162, 210 (1948). RUSSEL, C. Ann. Scienc. 19, 127 (1964).
Isso é um erro, e essa teoria de Berzelius, obsoleta. HUDSON, J. “The History of Chemistry. Electrochemistry and the Dualistic Theory.” Editora Springer,(1992). PULIDO, M.D.; PORTO, P.A. (Orientador), “O Dualismo Eletroquímico de Berzelius.” Dissertação de Mestrado em Ensino de Química, Instituto de Física, Universidade de São Paulo (2016). Outro Link.
Apesar disso, a “Teoria do Dualismo Eletroquímico” estava para ser ressuscitada, após a descoberta do elétron, pelo Físico Inglês Joseph John Thomson. SALTZMAN, M. J. Chem. Educ. 50, 59 (1973).
Como se sabe hoje, os ácidos são caracterizados por conterem hidrogênio, e não oxigênio. Isso foi antevisto por Humphy Davy, confirmado em 1838, pelo Químico Alemão Justus Freiherr Von Liebig e reconfirmado, assim como a ionização, pela “Teoria da Dissociação Eletroquímica” do Químico Sueco Svante August Arrhenius.
A muitos anos, se sabe que os metais reativos, eletropositivos “deslocam hidrogênio” dos ácidos minerais. Assim o hidrogênio gás pode se formar e o átomo de hidrogênio está na fila das tensões, como se fosse um metal.
Como vimos neste Artigo, Berzelius também modificou certas vidrarias de laboratório. O copo béquer atual, forma baixa e com bico, é o “Copo de Griffin” e a forma alta é o “Copo de Berzelius“.
O béquer alto de Berzelius, já aparece fabricado, J.J. Griffin & Sons, no livro/catálogo do Químico,Vidreiro, fabricante de aparelhos científicos e Editor Inglês John Joseph Griffin em 1877. GRIFFIN, J.J. “Chemical Handicraft.” Editora J.J. Griffin & Sons, Londres, Inglaterra, Pág. 149 (1877).
De Berzelius, também é um importante procedimento em Química. Ele divulgou e estendeu o uso corrente nos laboratórios, do “carvão ativo”, que havia sido descoberto e estudado pelo Farmacêutico e Químico Sueco Karl Wilhelm Scheele, entre 1773-1777.
Até hoje usamos carvão ativo, muito, como um eficiente produto para limpar e purificar, despoluir, compostos, gases, materiais e água. BUBANALE, S.; SHIVASHANKAR, M. Int. J. Eng. Tech. Res. 6, 495( 2017). HASSLER, J.W. “Active Carbon, the Modern Purifier.” Editora: Githens-Sohl Corporation, New York, EUA (1841).
8. MICHAEL FARADAY:
Um pouco de História sobre o Físico e Químico autodidata Michael Faraday, (1791-1867).
Filho de um ferreiro e de uma dona de casa, era muito pobre e teve uma educação simples e de nível primário. Aos 13 anos, foi trabalhar em uma livraria e oficina de encadernação, e lá pegou muito gosto pela leitura, e lendo, adquiriu muita cultura e começou a aprender Química e Física, principalmente sobre eletricidade.
Lia todos os livros de Ciências que encontrava em bibliotecas, e mesmo sem instrução superior, começou a frequentar a Universidade, e assistir aulas, palestras e conferências científicas, principalmente do Filósofo Inglês John Tatum e do célebre Físico e Químico Humphry Davy .
Fascinado por Ciência desde a infância, Faraday gastava boa parte do pouco que ganhava em utensílios de laboratório simples e reagentes, com os quais fazia experiências. Tornou-se um muito hábil experimentalista, até hoje considerado um dos melhores que já existiram.
Faraday trabalharia na livraria até 20 anos de idade. Aos 21, em 1812, escreve a Humphy Davy uma extensa carta de 300 páginas, comentando sobre as palestras que assistira e sobre diversos experimentos, e pede a ele para ser seu assistente no laboratório.
Impressionado com a cultura e o nível científico do jovem e sua excepcional habilidade experimental, Davy aceita o novo assistente. Um ano depois, Faraday estava aceito na prestigiada, competitiva e muito rigorosa Royal Society. Em 1815, se torna um conferencista e cientista. a partir de 1833, um professor, mesmo sem faculdade!
Com a aposentadoria de Davy, e seu falecimento em 1829, Faraday herdaria seu laboratório.
São grandes sua contribuições à Química.
Foi ele quem oficialmente descobriu o hidrocarboneto aromático benzeno em 1825. FARADAY, M. Phil. Trans. Roy. Soc. London 115, 440 (1825). FARADAY, M. Phil. Mag. 66 180 (1825). TYNDALL, J. “Faraday as a Discoverer.” Editora D. Appleton Co. New York, EUA, Pág 15 (1868).
Embora se saiba hoje, que o benzeno havia sido isolado 40 anos antes. SCHLENZ, H. Angew. Chem. 21, 2577 (1908). De acordo com HOFMANN, Ber. Dtsch. Chem. Gessel. 23, 1271 (1890), o benzeno já havia sido isolado pelo químico alemão Eilhardt Mitschelich.
Veja: TRIPP, E.H. Nature 115, 909 (1925). SOLLAS, W.J. Nature 115, 908 (1925). NEWELL, L.C. J. Chem. Educ. 3, 1248 (1926). KAISER, R. Angew. Chem. Int. Ed. 7, 345 (1968). WALDEN, P. Angew. Chem. 39, 125 (1926).
Também foi Faraday quem estudou os metais e as soluções coloidais, nos dias atuais, se diria materiais nanoparticulados. Inventou os vidros óticos, liquefez vários gases, estudou ligas metálicos e melhorou a Catálise, que havia sido descoberta por Berzelius, preparou os primeiros compostos não iônicos e orgânicos do cloro etc… etc… THOMAS, J.M. Chem. Commun. 53, 9179 (2017). THOMAS, J.M “Michael Faraday and the Royal Institute.” Editora Taylor & Francis, Londres, Inglaterra (1991).
O trabalho dele em Física é ainda mais extraordinário.
Descobriu o fenômeno da indução eletromagnética, inventou o transformador elétrico, o dínamo, o gerador e o motor elétrico, melhorou a pilha de Volta, inventou a Eletroquímica, que seria também estudada por Berzelius e Davy, Descobriu como se media a intensidade de corrente (“amperagem”), estudou os imãs e os magnetos etc… TRICKER. R.A.R. “The Contribution of Faraday ands Maxwell to Electrical Science.” Editora Pergamon Press, Oxford, Inglaterra (2013).
A descoberta da indução eletromagnética levaria às equações de Maxwell e ao aparelho de Rádio, de Hertz, Marconi, Landell de Moura e Nikola Tesla.
Pioneiro da Eletroquímica e da Eletrólise. Os termos “íon”, “eletrólise”, “ânodo”, “cátodo”, são dele
Faraday acreditava e postulou que todas as forças naturais, como gravidade, luz, magnetismo, energia química, eletricidade, calor etc… tinham uma origem comum, uma energia universal, e podiam ser reduzidas e resumidas à mesma coisa…Isso se chamava “Teoria do Campo Unificado“. Era algo muito inovador para a época, 1851. FARADAY, M. Phil. Trans. 141, Pág 1 (1851). Ibid, Pág 7, (1851). Ibid. Pág 29 (1851). Links: 206, 207, 208, 209, 210. 216 FORBES, M.; MAHON, B. (2014). WALSH, F.C. Bull. Electrochem. 7, 481 (1992). Links 217, 218, 219, 220.
Com o tempo, isso se mostrou só parcialmente verdadeiro. Por exemplo, luz e eletricidade são assemelhadas, mas não com a gravidade e magnetismo. Mas curioso notar que Faraday errou, mas passou perto…
Pode ser Filosóficamente e Matemáticamente correlacionado, e tem a ver com modificações da “Teoria da Relatividade” do muito famoso Físico Alemão Albert Einstein. Einstein procurou provar a “Teoria do Campo Unificado“ por 30 anos. Veja os trabalhos de Einstein. Link 211. Link 212. 213, 214, Links: 223, 224, 225, 226, 227.
Veja também “Teoria do Campo” de Einstein-Cartan-Evans, Myron W. Evans. (2003 a 2007). EVANS, M.W. “Generally Covariant Unified Field Theory.” (2005). ANDERTON, R.J. Gen. Scienc. J. 14, 1 (2012). HART, J.B (2005). Entretanto, os trabalhos de Evans link 16, são controversos e bem criticados, HEHL, F.W. Found. Phys. 38, 7 (2008). BRUN, G.W.; HEHL, F.W.; JADCZYUK, A. “Cornell University, Arquivo arXiv.” (2007). Link 215. Link 221. 222.
9. OUTROS QUÍMICOS:
Michel Eugène Chevreul:
Encerrando o Artigo, outros Químicos menos conhecidos, mas com um trabalho importante ou interessante.
O Químico Francês Michel Eugène Chevreul. Já falei dele ao tratar de experimentos com o “Sal de Chevreul“. Ele fez muitos outros trabalhos, mas dois se destacam.
Ele estudou as gorduras animais e os óleos vegetais.
Foi ele quem descobriu, ou melhor, confirmou, que as gorduras são triglicerídeos, isto é ésteres de ácidos carboxílicos com glicerol. CHEVREUL, M. E. “De la Methode a Posteriori Experimentale.” Editora Dunot, Paris, França (1870). CHEVREUL, M.E. “Recherches sur les Corps Grass D’Origine Animale.” Editora Levrault, Paris, França (1823). BERTHELOT, M. “Combinations de la Glycérine avec les Acides.” Editora Mallet-Bachelier, Paris, França, Págs. 5, 6, 32, 46, 49, 56, 70, 71, 98, 100, 103 etc… (1854).
Dizemos confirmou, porque gorduras e óleos são muito antigos, e a saponicação também. De fato, o sabão foi inventado pelos Babilônios, por volta de 2800 aC. Os Romanos o conheciam, e também usavam óleos essenciais para perfumá-lo. Os Egípcios usavam óleos vegetais, invés de gordura animal. Assim, gordura ou óleo eram saponificados com cinzas (que contém carbonatos de sódio ou potássio), para formar o sabão.
Conhecido na Alquimia, o sabão tinha até um símbolo para representá-lo.
A Glicerina (Glicerol) foi descoberta em 1783, outro link, pelo Alquimista (um dos últimos), Farmacêutico e Químico Sueco Carl Wilhelm Scheele. Ele estudava o envelhecimento, oxidação e endurecimento dos óleos vegetais por óxidos metálicos. São os “Óleos Secativos“, que hoje se usam para fazer tintas e vernizes.
Scheele tratou gorduras e óleos com litargírio, “Cal de Chumbo”, [PbO, óxido de chumbo (II)] e obteve um líquido que chamou “Princípio Doce das Gorduras“, pensando se tratar de um açucar, logo percebeu que não era, pois não fermentava e nem tinha, quando submetido a uma análise química, a mesma proporção de oxigênio (“Flogisto“). SCHEELE, K.W.; BARROIS, T. (Editor e Tradutor), “Memoires de Chymie, de la Académie Royale de Sciences de Stockholm, Traduits du Suédois e de L’Allemand.” Editora Livraria Cuchet, Paris, França, Págs 191-193 (1785).
Veja também: FREMY, M. Phil. Mag. 30, 42 (1908). SMEATON, W.A. Endeveour, 10, 28 (1986). RIGBY, E. “Chemical Observations on Sugar.” Editora Gráfica J. Johnson, Londres, Inglaterra (1788).
Foi Chevreul quem denominou o composto de glicerina, em 1811. DIJKSTRA, A.J.; LIBBEY J. (Editor), Core Eurotext, Inglaterra (2009). Outro link, NEUMANN, H.H.C.; JURGERMANN, E.; SONNTAG, N.O.V. (Editores) “Glycerin(e) and its History. Em Glycerine, AKey Cosmetic Ingredient” Pág. 7 (1991). CHEVREUL, M.E. Ann. Chim. 88, 225 (1813). CHEVREUL, M.E. Ann. Chim. 95, 5 (1815).
Até a época de Chevreul, não se tinha certeza se a glicerina fazia parte de todas as gorduras, se achava que só de algumas. BERTHELOT, M. “Combinations de la Glycérine avec les Acides.” Editora Mallet-Bachelier, Paris, França, Págs. 5, 6, 32, 46, 49, 56, 70, 71, 98, 100, 103 etc… (1854) . Chevreul confirmou que glicerina e ácidos graxos faziam parte de todas as gorduras, animais e vegetais. CHEVREUL, M.E. Ann. Chim. Phys. 2, 339 (1816). CHEVREUL, M.E Ann. Chem. Phys. 2, 16 (1823).
Assim ele estuda os óleos e gorduras, analisa, faz sabões e saponificações, e confirma algumas gorduras por síntese química, e estuda suas reações, e confirma que todos os óleos e gorduras naturais, vegetais ou animais contém ácidos graxos combinados com o glicerol. WISNIAK, J. Indian J. Chem Tech. 11, 140 (2004)
Também confirmou a existência da função orgânica “éter-sal“, chamada também de “êtal“, ela sabia que faziam parte das gorduras. Descobriu esses fatos através de muita Química Analítica nova, para a época. CHEVREUL, E. “Considerátions Générales sur L’Analyse Organique e sur ses Aplications.” Editora Levrault, Paris, França (1824). DIJKISTRA, A.J. Oleagineux, Corps Gras et Lipides, 16, 8 (2009). THENARD et CHEVREUL, “Rapport sur Une Memoire de M. Serullás.” Editora: Academie Royale de Sciences, Paris, França (1829). THOMSON, T. “Chemistry of Organic Bodies. Vegetables.” Editora J.B Bailliére & MAclachlan e Stewart, Londres, Inglaterra, Paris, França e Glasgow, Escócia (1838).
Sobre os “Êtais“, “Éteres-Sal“, eram confundidos com os éteres, por sua volatilidade. DUMAS, J.B.A.; PELIGOT, E. “Recherches sur La Nature de L’Ethal.” (1838). LASSAIGNE,M. Lond. Edin. Dub. Phil. Mag. J. Scienc.10, 420 (1837). ALDRIDGE, J. Dub. J. Med. Scienc. 16, 318 (1839).
Por exemplo, os “Éteres-Sal” aparecem em muitos trabalhos antigos. BAKER, H.J.; VAN DER BAAN, Rec. Trav. Chim. Pays Bas 56, 1161 (1937). LECOMTE, J.J. (1942). JAEGER, F.M. Rec. Trav. Chim. Pays Bas Belg. 25, 324 (1906). Hoje se sabe, são os ésteres, grupo funcional orgânico éster.
Os trabalhos de Chevreul revolucionaram e modernizaram a Química das gorduras e dos óleos e a indústria do sabão e das velas.
Outro importante trabalho de Chevreul. Ele estudou muitos corantes e tintas. CHEVREUL, M. Acad. Roy. Scienc. Mem. 16, 182 (1837). CHEVREUL, E. “Leçons de Chemie, Appliquée à la Teinture.” Editora Pichon et Didier, Paris, França, Vol. 1 (1829). CHEVREUL, M. “Recherches sur la Teinture.” Editora L Martinet, Paris, França, Vols. 1-3 (1842). CHEVREUL, M. “Recherches Expérimentales su la Peitnture a L’Huile.” Editora Tipografia Firmin Didot et Frères, Paris, França (1850).
E elaborou a chamada “Teoria das Cores“, combinações e harmonização das cores, algo importante em pintura artística inclusive. Também inventou os “Circulos Cromáticos” para combinar cores. CHEVREUL, M.E “Theorie des Effets Optiques que Présentent les Éttofes de Soie.” Editora F. Didot, Paris, França (1846). CHEVREUL, M.E. “De la Loi du Contraste Simultané des Couleurs et de L’Assortiment de Objets.” Editora Gráfica Pitois-Levrault, Strasbourg e Paris, França (1839). CHEVREUL, M.E. “Des Couleurs et de Leurs Applications aux Arts Industriels, a L’Aide des Circles Chromatiques.” Editora J.B Baillière et Fils, Paris, França (1864).
Links sobre o trabalho de Chevreul com as cores. Links: 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244,245, 246, 247 ,248.
Assim, embora tenha feito muitas coisas em Química, a importância maior e a fama de Chevreul advém principalmente de seu trabalho com as gorduras , links: 249, 250, 251, e as cores.
Louis Nicolas Vauquelin:
Farmacêutico e Químico Francês, Louis Nicolas Vauquelin, Link: 252. Extensa biografia dele.
Foi aluno do Químico, ex Flogista e seguidor de Lavoisier, o Francês Antoine François de Fourcroy. E ele próprio, Vauquelin, foi professor de Chevreul.
Em toda a sua carreira Fourcroy foi sempre mais famoso. o Mérito de Vauquelin somente foi totalmente reconhecido após a sua morte. DORVEAUX, P. Rev. Inst. Pharm. 78, 57 (1932).
Porém alguns Químicos da Europa, reconheciam o mérito dele, considerando-o um grande Químico. MORETTI, J. “Memorie ed Osservazioni Intorno a Diversi Oggeti Risguardanti le Scienze Naturalli.” Tradução Livre do Título: “Memórias e Observações sobre Diversos Assuntos Pertencentes às Ciências Naturais.” Editora: Tipografia Pietro Bizzoni, Pávia, Itália, Vol. 1 Págs. 6, 8, 136, 201 (1820). VON LIEBIG, J.; VANZANI, G. (Tradutor), “Trattato di Chimica Organica di Giusto Liebig.” Editora Angelo Bonfanti, Milão, Itália, Págs. 51, 169, 443, 506, 540 (1844).
Vauquelin descobriu 2 elementos químicos, na época novos, o cromo e o berílio. Também isolou os primeiros aminóácidos e o alcalóide do tabaco, a nicotina.WISNIAK, J. Rev. CENIC Cienc. Quim. 34, 47 (2003). VAUQUELIN, L.N.; ROBIQUET, P.J. Ann. Chem. 57, 14 (1806), citado por: GU, SX et al., Pharm. Fronts, 2, e79 (2020). SPIESSER, N. Bull. Union Phys. 807, 1403 (1998).
Junto com Fourcroy, ele denominou o resíduo da platina de “Pteno“, mas não conseguiu separar dele, dois elementos químicos novos, o irídio e o ósmio. HAUBRICHS, R.; ZAFFALON, P.L. John. Matt. Technol. Rev. 61, 190 (2017).
Mas a maior contribuição de Vauquelin foi para a Química Analítica TOMIC, S. Compt. Rend. Chimie, 15, 553 (2012).
Principalmente a Qualitativa, seja de minerais como de compostos orgânicos ou naturais. VAUQUELIN, L.N. “Analyse de la Matière Cérébrale de L’Homme e de Quelques Animaux.” Editora Didot Jeune, Paris, França (1811).
Por exemplo, Vauquelin e Chevreul descobriram que soluções de oleatos, estearatos alcalinos ou de sabão, formam precipitados com sais de metais de transição, de cor característica do metal. O sabão seria então, um reagente útil e barato. WISNIAK, J. Indian J. Chem Tech. 11, 140 (2004).
Funciona e funciona bem! Com sabão de côco, eu fiz experimentos assim, quando estudava Química. (FEDERMAN NETO,A., 1975). As cores dos sais insolúveis formados são muito bonitas. Experimente adicionar uma solução hidroalcoólica de sabão de coco, a tubos de ensaio contendo soluções de cloretos ou sulfatos de cobre, ferro (II), ferro (III), níquel ou cobalto.
Principalmente a Qualitativa, seja de minerais como de compostos orgânicos ou naturais. VAUQUELIN, L.N. “Analyse de la Matière Cérébrale de L’Homme e de Quelques Animaux.” Editora Didot Jeune, Paris, França (1811).
Sabe aquelas reações de tubos de ensaio, que os químicos e estudantes fazem, até no segundo grau? Reações dos cloretos, dos sulfatos, dos cromatos etc.. e dos cátions, ferro, cromo, cobalto, níquel, manganês etc… São os famosos “Ensaios de Cátions e Ânions” que estão em todos os livros didáticos de química e de ciências…
Pois é, foi Vauquelin quem inventou os primeiros ensaios de cátions e ânions. Links: 253, 254, 255, 256, 257, 258, 259, 260, 261.
VAUQUELIN, L.N.; ARCET, J.P.L (Revisor) “Manuel de L’Essayer.” Editora Bernard, Paris, França (1799). Outra Edição completa e revista: VAUQUELIN, L.N.; ARCET, J.P.J.; VERGNAUD, A.D.; GAY-LUSSAC, J.L. (Revisores) “Manuel Complet de L’Essayer.“, tradução Livre do Título: “Manual Completo do Analista.” Editora Roret, Paris, França (1836). Ibid, Nouvelle Edition (1836).
10. CONCLUSÃO:
Neste Artigo, vimos a História de alguns Químicos pioneiros e famosos do passado, e seu trabalho inovador, que resultou em muitos desenvolvimentos Científicos e Tecnológicos.

