Autor: Alberto Federman Neto, AFNTECH.
Atualizado em 14 de Junho de 2019.
Embora eu já tenha publicado neste Blog, um Artigo sobre outros compostos de cobre, o Sal de Chevreul tem aspectos interessantes e diferentes, que justificam estudá-lo em separado.
1. Introdução e História.
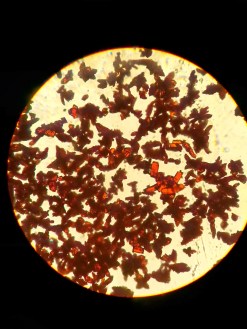
A imagem que ilustra este Artigo. São cristais de Sal de Chevreul, vistos ao microscópio. Fonte da Imagem: The Home Scientist , Blogspot. 2013.
O que vem a ser “Sal de Chevreul“? É um sulfito duplo de cobre (I) e cobre (II) na mesma molécula, fórmula molecular CuSO3.Cu2SO3.2H2O ou Cu3(SO3)2.2H2O, obtido na forma de pequenos cristais vermelhos, insolúveis em água.
Ele foi descoberto pelo Químico Francês Michel Eugène Chevreul., em 1812, através da reação entre o “sulfito de potássio” e o sulfato de cobre (II). CHEVREUL, M.E. Ann. Chim. 83, 181 e 187, 1812. A luz do conhecimento atual, o “sulfito de potássio” usado é metabissulfito de potássio. K2S2O5.
O Sal de Chevreul também pode ser feito com o metabissulfito de sódio, invés do sal de potássio. Veja links de protocolos modernos de fazer o sal de Chevreul: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 , 18, 19 , 20 , 21 , 22. Também sulfitos neutros de sódio ou amônio, (NH4)2SO3, podem ser usados. OMORI, K.; OKUWAKI, A.; SUZUKI, T.; ITO, H.; OKABE.T. Bull. Chem. Soc. Japan 39, 78, 1966. Link 2.
Também pode ser feito sob pressão, método hidrotérmico., em meio ácido, ou pela reação entre sulfato de cobre (II) e gás sulfuroso, SO2. (ÇALBAN, T.; KUSLU, S.; ÇOLAK, S. Chem Eng. Comm. 196, 2018, 2009) Ou a partir de cobre metálico.
2. Outros Trabalhos Importantes de Chevreul.
Esse Químico Francês fez muitas descobertas e desenvolvimentos científicos.
Eu, quando era estagiário no IPT (FEDERMAN NETO, 1977), descobri que soluções hidro alcoólicas de sabão de coco formavam sais insolúveis com soluções de metais de transição, e esses sais tinham a cor característica, para cada metal, identificando-o.
Na composição do óleo de coco, predominam os ésteres do ácido láurico [fórmula molecular 3HC-(CH2)10-COOH]. SILVA NETO, N. et cols. Comunicação, “Quinto Congresso Norte-Nordeste de Química”, Associação Norte-Nordeste de Química. Natal, 2013.
Portanto. a solução de sabão de coco, pode ser considerada como de laurato de sódio.
Na época, eu não sabia (era mais difícil localizar literatura científica). Mas Chevreul já tinha feito experimentos semelhantes aos que eu fiz.
Embora o sabão, preparado emṕíricamente, seja conhecido desde a antiga Babilônia e o Egito, foi Chevreul quem o estudou científicamente, 1813-1826, Links 2, 3, 4, 5. E às gorduras, principalmente animais. WISNIAK, J. Educ. Quím. 13, 133, 2002. DEFFENSE, E. OCL, 16, 14, 2009.
Foi ele quem descobriu que as gorduras são ésteres de ácidos graxos com glicerol, e sua saponificação forma sais de sódio ou potássio, dos ácidos graxos, os sabões.
Em resumo, Chevreul estudou em profundidade e detalhes, esclarecendo a Química das gorduras e dos sabões. CHEVREUL, M.E. Ann. Chim. 88, 225, 1813. CHEVREUL, M.E. “Recherches Chimiques sur les Corps Gras D’Origine Animale.” Editor: LEVRAULT, F.G., Strasbourg, França, 1823. Link 2. Também inventou o primeiro tipo de Margarina, feita com gordura animal. CHEVREUL, M. Phil. Mag. 44, 193, 1814.
Já o grupo funcional, função orgânica, éster . O Quimico Francês Jean Baptiste André Dumas preparou os ésteres em 1828, mas assim como Berzelius, preferiu considerá-los como derivados dos éteres e os chamou éteres-sal.
Esse nome permaneceu usado ainda por muito tempo. Por exemplo, aparece em um livro do Autor deste Blog, ENGEL, R. “Traité Elementaire de Chemie.” Librairie J.R Bailliére, Paris, França, Parte IV, Pág. 225, 1896.
Já a esterificação, preparação moderna dos ésteres, pela reação entre álcoois e ácidos carboxílicos, foi desenvolvida pelo Químico Alemão Hermann Emil Louis Fischer, em 1895. FISCHER, E.; SPEIER, A. Ber. Deutsch. Chem. Gessel. 28, 3252, 1895.
Foi o Químico Alemão Leopold Gmelin, quem, em 1848, pela primeira vez chamou o grupo de éster. GMELLIN, L. “Handbuch der Organische Chemie.”, Heidelberg, Alemanha, Pág. 182, 1848.
Chevreul também fez muitas contribuições para a Arte, não só para a Química.
Ele desenvolveu a Teoria das Cores. Aperfeiçoou os trabalhos de Goethe e Isaac Newton, sobre as cores. Links: 2, 3, 4 , 5, 6, 7, 89. Estudou contrastes, harmonia entre as cores etc… Descobriu as “Cores Básicas e Complementares” e inventou os “Círculos Cromáticos“. HEILA, E. Color Res. App. 16, 198, 1991. ROQUE, G. “Encyclopedia of Color Science and Technology.” 2015. Link 9. DIGEON, R.H. “Cercles Chromatiques de M. E. Chevreul.” Editor DIGEON, Paris, França, 1855. CHEVREUL, E.G. “De la Loi du Contraste Simultanée des Couleurs. 1839. MARTEL, C. Tradução para o Inglês da obra de Chevreul. Longman, Brown, Green & Longmans, 2 Edição, 1855. OSBORNE, R. Leonardo, 21, 96, 1988.
Também estudou a Hipnose, e desmistificou o velho pêndulo dos ocultistas, relacionando-o à Psicologia. “Pêndulo de Chevreul“. Link 2, 3, 4, 5, 6, 7, 8.
3. Bissulfito de Sódio e Metabissulfito de Sódio.
Aqui uma observação. Por influência de uma antiga nomenclatura, metabissulfitos de sódio ou potássio são às vezes, chamados de bissulfitos.
No estado sólido, no frasco de reagente, eles não são o mesmo composto! O bissulfito de sódio tem fórmula NaHSO3, e o metabissulfito de sódio, é o pirosulfito, Na2S2O5.
Mas dissolvidos em água, os metabissulfitos sofrem hidrólise, se dissociam, e a solução formada será a de bissulfito.
Na2S2O5 + H2O = 2 NaHSO3
Resumo, não são o mesmo sulfito, no sólido, mas são, quando em solução aquosa.
Mas o metabissulfito também pode formar o sulfito neutro, por aquecimento. Link 2.
4. Testes Preliminares.
Em testes preliminares, verifiquei ser possível usar metabissulfito de sódio, invés do de potássio. O Sal de Chevreul também se forma.
Porém, quando usei metabissulfito de sódio, às vezes, preferi adicionar um equivalente molar ou excesso, de sulfato de potássio. Isso porque é conhecido que sem íons de potássio, há uma tendência a perder parte do cobre (I), do Sal de Chevreul formado, por “metátese”, troca de íons, visto que íons de sódio e cobre (I) tem aproximadamente, o mesmo tamanho. SILVA, L.A.; ANDRADE, J.B. J. Bras. Chem Soc. 15, 170, 2004.
Pelo exposto no Item 3, era de se esperar que bissulfito de sódio poderia substituir o metabissulfito. De fato isso ocorre. O Sal de Chevreul se forma também, usando bissulfito.
Outra observação que faço: Ao misturar as soluções de sulfato de cobre com o metabissulfito, mas antes de ferver, forma-se uma solução verde clara límpida, link 2, ou um precipitado amarelado, que ainda não é o sal de Chevreul. Ao que parece, a natureza dessa solução verde, ou precipitado amarelado, não é conhecida. Link 2.
Especulo que esse precipitado amarelo, cuja solução é verde, possa ser o sulfito neutro de cobre (I), Cu2SO3, ou seus complexos, o “Sal de Étard“, chamado por Chevreul “sulfito amarelo de cobre”. ETARD, M.A. Compt. Rend. Acad. Scienc. 94, 1422, 1475, 1882. CHEVREUL, M.E. Ann. Chim. 83, 181 e 187, 1812 , DASENT, W.E.; MORRISON, D. J. Inorg. Nucl. Chem. 26, 1122, 1964. Link 2. Também pode ser um sulfito duplo, o Cu2SO3.K2SO3, veja exemplos: HABASHI, F.; DUGDALE, R. Metall (Berlin), 28, 129, 1974. CONKLIN, M.H.; HOFFMANN, M.R. Environ. Scienc. Technol. 22, 883, 1988.
Mais experimentos:
Embora tenham sido descritos vários protocolos modernos para obter o Sal de Chevreul (veja Ítem 1), de acordo com ÇALBAN et cols., mais fácil operar com sulfito neutro (embora eles usem sulfito de amônio ou sódio) , a 60-70 graus, por 15-30 min. E o pH ajustado a 3-4. ÇALBAN, T.; SEVIN, F.; LAÇIN, O. Int. J. Chem. Mol. Eng. 10, 1021, 2016. ÇALBAN. T.; KAYNARCA, B.; SEVIM, F.; EROGLU, H. Asian J. Chem. 26, 6111, 2014. ÇALBAN, T.; YESILYURT, M. Inz. Chem. Proc. 28, 85, 2007. ÇOLAK, S. et cols. Powder Technol. 134, 65, 2003. ÇALBAN, T.; LAÇIN, O.; KURTBAS, A. Int. J. Chem. Mol. Eng. 9, 385, 2015.
Também existem preparações otimizadas usando bisulfito de sódio: INOUE, M.; GRIJALVA, H.; INOUE, M.B.; FERNANDO, Q. Inorg. Chim. Acta 295, 125, 1999.
Vamos aos experimentos, as tentativas de otimização:
Dissolver 11 g (cerca de 0.05 mol) de metabissulfito de potássio, em 60 ml de água. Neutralizar com carbonato de potássio (5,5 g, cerca de 0,025 mol), para formar o sulfito neutro, K2SO3. Reservar.
Em outro frasco, Dissolver 12,5 g (cerca de 0,05 mol) de sulfato de cobre pentahidratado, em 60 ml de água. Reservar.
Misturar as duas soluções. Forma-se uma solução verde. Aquecer a mistura a 70-80 graus. O precipitado de sal de Chevreul se forma. Deixe esfriar. Filtrar, ou decantar o sal de Chevreul, lavar bem com água fria e secar ao ar.
Mesmos resultados ao repetir protocolos conhecidos, ou usando quantidade equivalente de metabissulfito de potássio, a 60-70 graus, ou mesmo fervendo. Links: 1, 2, 3, 4, 5.
Invariavelmente, neutralizando ou não, notei que sempre o sal de Chevreul se separa escuro, marrom, quase preto, e nunca vermelho! E parece sobrar cobre livre na solução.
Há reportos em literatura, de precipitação de sal de Chevreul, em forma de sólido marrom escuro, quase preto . Link 2. YOUZBASHI, A.A.; DIXIT, S.G. Metallurg. Trans., B. 24, 563, 1993.
Identifiquei que a solução azul, contem cobre (II), detectado por reação com amoníaco aquoso (amônia). Também contém sulfato (reação positiva com cloreto de bário), mas quase não contém mais sulfito. Cobre também pode ser detectado pela reação com brometo de potássio em presença de ácido fosfórico. Reagente de Dishon-Goldschmidt. GOLDSCHMIDT, F.; DISHON, B.R. An. Chem. 20, 373, 1948.
Tenho em mente que o excesso de cobre que restou oxidou o sulfito a sulfato e o precipitado preto é sal de Chevreul, mas impurificado com óxido de cobre (II), CuO.
Em alguns artigos e links (já citados aqui) reporta-se que o meio ácido é vantajoso. pH 3 ou 4. Acertei o pH da mistura com ácido sulfúrico diluído. Nesse caso, o Sal de Chevreul se forma, avermelhado, mas a reação é bem mais lenta.
Em outro experimento, acidulei a mistura com ácido acético, como recomendado por GUAN et cols. Aliás , eles partem de acetato de cobre (II) e sulfito neutro de sódio, a temperatura ambiente, e acidulam com ácido acético. O método deles, eu chequei, é reprodutível. GUAN, M.; JIAN, Y.; SUN, J.; CHANG, T.; LIU, Q.. XU, Z. Cryst. Eng. Comm. 38, 1044, 2015. Link 2.
Em testes iniciais, eu usei sulfato de cobre (II) e metabissulfito de potássio, em pH regulado a 3-4 com adição de ácido acético. A reação funciona, mas o Sal de Chevreul vermelho que se separa, fica marrom com grande aquecimento, e a solução fica alcalina.
Especulo do que pode estar acontecendo. Meus frascos dos metabissulfitos, por serem velhos, absorveram gás carbônico da atmosfera, e agora contém carbonato, por isso, o PH se altera e óxido de cobre (II) é formado.
Em todo o caso, adição de ácido acético parece ser muito vantajosa, pois o carbonato (impureza) foi neutralizado.
5. Otimização da Preparação do Sal de Chevreul.
Método de GUAN et cols., traduzido e transcrito, testado, funciona. O material obtido é coloidal, nano particulado.
Adicionar 20 ml de solução de sulfito neutro de sódio, concentração de 7,6 mmol/L, a 20 ml de numa solução de acetato de cobre monohidratado, 4,67 mol/L, Forma-se uma solução verde. Agitar por 15 min. Adicionar 5 ml de ácido acético.
Agitar a temperatura ambiente. Espere todo o sal de Chevreul, avermelhado, se depositar. Interrompa a agitação, filtre e lave o sólido com água. Seque em estufa a vácuo, a 80 graus Celsius.
Meu método, baseado no Método de GUAN et cols e vários outros protocolos gerais.
Dissolver 9,5 g de sulfato de cobre pentahidratado em 100-120 ml de água. Reservar. Dissolver 9.5 g de metabissulfito de potássio (se usar metabissulfito de sódio, são 8 g, mas junte 1 g de sulfato de potássio), em 40-50 ml de água. Fiz testes também com estas proporções de reagentes, e estas, com bons resultados.
Misturar as duas soluções. Ajustar o pH a 3-4, com ácido acético glacial. Deixar em repouso a temperatura ambiente, ou aquecer levemente, máximo de 60 graus.
Notará que o Sal de Chevreul se separa avermelhado, gradualmente. Quando o precipitado se formou, filtre ou decante e lave com água e seque ao ar.
O Sal de Chevreul se separa na forma de cristais avermelhados, insolúveis em água. A cor é parecida com a do pó de cobre.
Reação que ocorre. Basicamente, é uma redução parcial do cobre pelo sulfito. Águas de Cristalização incluídas. Em negrito, está a fórmula molecular do Sal de Chevreul, Veja: SILVA, L.A.; ANDRADE, J.B.; MANGRICH, A.S J. Bras. Chem. Soc. 18, 607, 2007. Para as equações parciais, veja aqui.
3 CuSO4.5H2O + 4 K2S2O5 = CuSO3.Cu2SO3.2H2O + 4 K2SO4 + 5 SO2 + 3 H2O
Identificar o sal de Chevreul. Dissolver um pouco, em ácido clorídrico cerca de 10 % (é ácido concentrado dissolvido com 2 volumes de água).
Diluir a solução clorídrica com água ou água e sal. Forma-se um precipitado branco de cloreto cuproso (CuCl). Prova que existe cobre de valência (I) no composto.
Diluir outra amostra em amoníaco (amônia aquosa), 1:2 v.v. Forma-se uma solução azul forte, contendo o cátion complexo tetramincobre. [Cu(NH3)4]+2. Isso identifica cobre de valência (II).
Para identificar o sulfito, dissolva o Sal de Chevreul em ácido clorídrico concentrado, em um tubo de ensaio pequeno, 10×10 ou 10×12. Na boca do tubo, coloque um pedaço de papel de filtro molhado em solução de dicromato de potássio. a formação de uma coloração verde no papel (redução do dicromato) , é prova positiva para sulfito.
6. Características do Sal de Chevreul.
O que torna o Sal de Chevreul tão interessante?
Ele tem 3 átomos de cobre, em valências diferentes, Cobre (I) e Cobre (II), no mesmo composto!. É um exemplo do que se chama em Química, compostos de “Valência Mista“. ROCHA, R.C.; TOMA, H.E. Quím. Nova, 25, 624, 2002. ROBIN, M.B.; DAY, P. Adv. Inorg. Chem Radiochem. 10, 247, 1968. YOUNG, C.G. Coord. Chem. Rev. 96, 89, 1989.
No espectro eletrônico do Sal de Chevreul, existe uma banda de transferência de carga a 425 nm, entre os átomos de cobre (I) e os ligantes sulfito, metal-ligante ou ligante metal.
Também uma importante banda, movimento de elétrons, entre os átomos de cobre (I) e cobre (II). Essa banda ocorre a 500 nm, faixa do azul , portanto o composto reflete vermelho… Por isso, o Sal de Chevreul é vermelho. SILVA, L.A.; ANDRADE, J.B.; TOMA, H.E. J. Bras. Chem Soc. 13, 624, 2002.
Resumo… ao mesmo tempo que cada átomo de cobre tem valência (I), também tem valência (II). Essa banda a 500 nm, é um exemplo do que se chama: “Banda de Intervalência“. Um movimento de elétrons entre os átomos de cobre, interna à molécula.
7. Confirmando essa Banda de Intervalência.
Para confirmar, vamos geral uma solução de cobre que tenha um “movimento de elétrons” semelhante. Pode-se usar uma solução de cobre na valência três, cobre (III).
A existência da rara valência (III) do cobre, foi descoberta pelo Químico Francês Léon André Jean Eugène Malaprade, em 1937. MALAPRADE, L. Compt. Rend Hebdo. Sceanc Acad. Scienc. 204, 979, 1937. LEVASON, W.; SPICER, M.D. Coord. Chem. Rev. 76, 45, 1987. UPRETI, D.D.; MISHRA, R.; AGARWAL, R.P. Inorg. Chim. Acta, 45, L221, 1980.
Vamos obter uma solução de íons de cobre na valência (III). Em um tubo de ensaio, trate uma solução de sulfato de cobre (II) com dois fortes oxidantes: metaperiodato de sódio ou potássio (Links 2, 3, 4, 5), e persulfato de potássio, amônio (link 6) ou sódio. Veja, por exemplo: SINKOV, S.I; LUMETTA, G.J. Radiochim. Acta, 103, 541, 2015.
Observe a cor vermelha dessa solução. É porque ela tem intervalência entre os átomos de cobre, um “movimento de elétrons”, similar ao do Sal de Chevreul. WINTERTON, N. Roy. Soc. Chem Ann. Rep. A. 96, 26, 2000.
A solução formada é de Na5[Cu(HIO6)2], diperiodato cuprato de sódio. BALIKUNGERI, A.; PELLETIER, M.; MONNIER. D. Inorg. Chim. Acta, 22, 7, 1977.
7. Resultados, Discussão e Conclusão.
Um novo protocolo experimental para preparar o Sal de Chevreul a partir de sulfato de cobre e matabissulfitos de sódio ou potássio, é descrito. Ele é baseado em procedimentos conhecidos, mas incluindo controle de pH a 3-4 (com ácido acético).
Quando metabissulfito de sódio foi usado, adicionou-se sulfato de potássio para evitar metátese entre os cátions de sódio e cobre (I).
Geralmente, o Sal de Chevreul, [um sulfito duplo de cobre (I) e (II), de valência mista].
Em que pese sua complexidade e estrutura não usual, é considerado muito fácil de obter, basta ferver soluções de sulfato de cobre com sulfitos neutros, bissulfitos ou metabissulfitos.
Porém, em meus testes, notei que frequentemente, não precipita com a cor avermelhada, e sim, marrom (até preto, se tiver impurezas de CuO).
Isso porque a cor dele é muito sensível ao tamanho da partícula, tanto que ele fica mais alaranjado ao ser triturado. Link 2. e os cristais grandes são bem vermelhos.
Para obter a cor característica, não é tão fácil, principalmente se você usar amostras de metabissulfitos velhas e impurificadas com carbonatos.
Após muitos experimentos, descobri que a melhor maneira é controlar o pH (a 3-4) da mistura reacional de sulfato de cobre e metabissulfito, por adição de ácido acético.
E fazer a precipitação na menor temperatura possível, máximo de 60 graus Celsius. A temperatura ambiente, a reação demora bastante, mas invariavelmente, o Sal de Chevreul precipita avermelhado. Também é bom secar ao abrigo da luz, pois o sal é um pouco fotossensível.
Meu protocolo está descrito no Item 5.
O composto, descrito frequentemente como vermelho, é na realidade, castanho avermelhado, com cor semelhante à do cobre metálico. A cor é devida a uma “intervalência“, um movimento de elétrons entre os átomos de cobre (I) e (II) nesse composto, de valência mista.
Ao misturar o sulfato de cobre (II) com o metabissulfito, forma-se uma solução verde, límpida, o que indica uma redução instantânea a cobre (I), mas a natureza desse sal verde, não é conhecida. Estou tentando identificá-lo.

Ao começar a aquecer, ou deixar em repouso, começa a se formar um precipitado inicialmente amarelado e leve, que flutua, (Links 2 , 3) (porque o Sal de Chevreul, que se formará depois, é mais denso).

É o que Chevreul chamava de “sulfito amarelo de cobre”. CHEVREUL, M.E. Ann. Chim. 83, 181 e 187, 1812 .Trata-se do sulfito de cobre (I) hidratado, o Sal de Étard, estudado pelo Químico Francês Alexandre León Etard. ETARD, A. Compt. Rend. Acad. Scienc. 94, 1422, 1475, 1882 Tem fórmula molecular CuSO3.1/2H2O. BRANT, P.; FERNANDO, Q. J. Inorg. Nucl. Chem. 40, 235, 1978.
Étard ficaria muito mais famoso pela descoberta da “Oxidação de Étard“, com cloreto de cromilo, CrO2Cl2, Link 2, e outras oxidações relacionadas, efetuadas por compostos de cromo (VI). ETARD, A. Compt. Rend. Acad. Scienc. 90, 534, 1880. ETARD, A. Ann. Chem. Phys. 22, 218, 1881.
A Étard, foi também atribuída a descoberta do cloreto de cromilo, mas o composto é bem mais antigo, foi descoberto pelo Sueco Jons Jacob Berzelius em 1824, e estudado por Mendeleiev. BERZELIUS, J.J. Ann. Phys. Chem. 1, 34, 1824. HARTFORD, W.H.; DARRIN, M. Chem. Rev. 58 1, 1958.

