
Autoria: Alberto Federman Neto, AFNTECH
Revisto e Ampliado em 6 de Dezembro de 2022.
1. INTRODUÇÃO:
Neste Artigo, Química do sistema organometálico Ferroceno. E alguns experimentos relativamente simples com ele, e compostos relacionados.
Esses experimentos são diferentes do usual, e são interessantes como práticas de Química Inorgânica ou Orgânica, em cursos de Graduação e mesmo de Pós-Graduação.
No Artigo anterior, vimos a História do Ferroceno, sua estrutura química e reatividade em geral, como um substrato organometálico aromático..
E vimos que a Química desse sistema é o assunto da minha Tese de Doutorado, e minha principal linha de pesquisa, Química Organometálica. Veja Wikipedia.
2. OBTENÇÃO DO FERROCENO SEM SUBSTITUINTE:
Ferroceno é composto comercial e importante, tem inúmeros usos químicos e tecnológicos. Embora a preparação dele em laboratório, não seja compensadora, eu revisei os métodos de síntese.
Industrialmente é obtido em grandes quantidades, por reação entre ferro metálico e diciclopentadieno, ou ferro metálico, diciclopentadieno , e monóxido de carbono.
Na bonita imagem abaixo, cristais triclínicos de ferroceno, ao microscópio, Fonte da Imagem: TANAKA, R. Site Tumblr, Blog We Are Star Stuff, CenChemPics, (2016).

Outra Imagem. Fonte Shutterstock e OHRSTROM, L, “Chemistry World, Royal Society of Chemistry” , Londres. Inglaterra (2013).

Sumário dos métodos para preparar ferroceno sem substituinte, em laboratório.
Em laboratório (métodos antigos) , ferroceno pode ser preparado. BIRMINGHAM, J.M. Adv. Organomet. Chem. 2, 365 (1965).
Por reação entre o Reagente de Grignard do ciclopentadieno e cloreto férrico (método original). Ciclopentadienil sódio e cloreto férrico. PAUSON, P.L. J. Am. Chem. Soc. 76, 2187 (1957). Cloreto ferroso e ciclopentadieneto de sódio. RAUSCH,M.D.; VOGEL, M.; ROSENBERG, H. J. Chem. Educ. 34, 268 (1957). WILKINSON, G. Et. Al. Org. Synth. 36, 31 (1963) . Cloreto Ferroso e ciclopentadieno, usando alcóxidos de sódio como base. LITTLE, W.; KOESTLER, R.; EISENTHAL, R. J. Chem. Soc. 25, 1435 (1960).
Ciclopentadieno, cloreto ferroso e uma amina para desprotonar o ciclopentadieno (Método da Amina, Para Preparar Ferroceno). PRUET, R.L.; MOREHOUSE, E.L. Adv. Chem. 23, 1959 (1959). Texto Completo. TRIFAN, D.S.; NICHOLAS, R. J. Am. Chem. Soc. 79, 2746 (1957). WILKINSON, G. Et Al. Org. Synth. 36, 31 (1956). SHEATS, J.E.; RAUSCH, M.D. J. Org. Chem. 35, 3245 (1970). SHEATS, J.E.; HLATKY, G.; OLIVEIRA, S.M Quím. Nova, 6, 49 (1983). WATANABE, H. Et Al. Bull. Chem. Soc. Japan 38, 853 (1965). BIRMINGHAM, J.M.; SEYFERTH, D.; WILKINSON, G. J. Am. Chem. Soc. 76. 4179 (1954).
Reagente de Grignard do ciclopentadieno e complexos de ferro. WILKINSON, G. J. Am. Chem. Soc. 74, 6148 (1952). Cloreto ferroso, ciclopentadieno e etóxido de sódio como base. LITTLE, W.; KOESTLER, L.; EISENTHAL, R. J. Org. Chem. 25, 1435 (1960).
Métodos modernos: LARICK, F.A. Et Al. App. Organomet. Chem. 31, e3664 (2017).
Reação entre ciclopentadienil tálio e cloreto ferroso, eu trabalhei com essa reação. MACKHAEV, V.D.; BORISOV, A.P.; PETROVA, L.A. J. Organomet. Chem. 590, 222 (1999). FEDERMAN NETO, A.; BORGES, A.D.L. MILLER, J.; DARIN, V.A. Synth. React. Inorg. Metall-Org Chem. 27, 1299 (1997). FEDERMAN NETO, A.; BORGES, A.D.L. Quím. Nova, 21, 214 (1998).
Em todo o caso, um único método moderno de síntese do ferroceno sem substituinte ainda é usado, mas como prática eventual de Química Inorgânica. O “Método de Jolly” e suas modificações. JOLLY, W.L.; CAREY, N.A.D.; CLARK, H.C. Inorg. Synth. 11, 120 (1968). JOLLY, W.L.”The Synthesis and Caractherization of Inorganic Compounds.” Editora Prentice-Hall International Inc., Londres, Inglaterra e Englewood Cliffs, Ney Jersey, EUA, Págs.: 5 e 484 (1970). Outro Link. Tenho uma cópia impressa desse excelente livro.
Ciclopentadieno é desprotonado com hidróxido de potássio e reage com cloreto ferroso dissolvido em dimetilsulfóxido.

Embora o método seja muitas vezes usado como prática de química, pela sua didática e simplicidade…
A preparação laboratorial de ferroceno sem substituinte não compensa financeiramente, pois o melhor rendimento só é conseguido usando dimetoxietano (mais caro que o próprio ferroceno) como solvente. Gasta-se 50 ml de dimetoxietano para obter apenas 10 g. de ferroceno.
Éter e tetrahidrofurano , pentano, ou hexano podem ser usados, mas são menos eficientes.
Se você quiser conhecer esse método de importância didática, consulte estes links e vídeos: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30. 36. 37. 38. 49. 50. 105.
Eu fiz algumas vezes, quando não tinha ferroceno sem substituinte, disponível no laboratório, mas embora não seja composto barato, é melhor comprá-lo do que fazer.
Um frasco pequeno dá para fazer todos os experimentos aqui descritos, se a escala foi diminuída. Comprar ferroceno: 31, 32, 33, 34,
Por ser meu material de partida principal, tenho boa quantidade de ferroceno, de grau técnico, 97 % ou puro, 99 %, de várias marcas: Aldrich, Strem, Acros e Fluka. Se quiserem, comentem neste artigo, ou entrem em contato no meu email
Se for possível por correio, posso até fornecer pequenas quantidades.
Vamos usar ferroceno aqui, em alguns experimentos.
3. PURIFICAÇÃO DO FERROCENO SEM SUBSTITUINTE:
Em pequenas quantidades, ferroceno pode ser purificado por sublimação (várias referências). JACOBS, M.H.G.P. Et Al. J. Chem. Therm. 15, 619 (1983). WIKAL, W.M.; WEEKS, B.L. Talanta, 125, 24 (2014). Links: 35, 39, 40, 41, 42. Também por sublimação a vácuo. 43, 44, 45, 46, 47, 48, 49. 51.
Outra possibilidade para pequenas quantidades, é empregar cromatografia de coluna. Links: 51, 52, 53, 54, 55, 56, 57, 58, 59. GILBERT, J.C.; MONTI, J. Chem. Educ. 60, 369 (1973). BIRDWHISTELL, K.R. Et Al. 85, 261 (2008). WADE Jr., L.G. J. Chem. Educ. 55, 208 (1978). NAUMIEC, G.R. Et Al. J. Chem. Educ. 90, 376 (2013). SOUTHAM, D.C. Et Al. Chem. Educ. Res. Pract. 14, 476 (2013).
Porém para usar ferroceno comercial, como material de partida, é melhor purificar quantidadades maiores, e por recristalização.
4. EXPERIMENTOS:
Experimento 1. Recristalização de Ferroceno:
Porém para usar ferroceno comercial, como material de partida, é melhor purificar quantidades maiores, e por recristalização.
Literatura geral reporta que ferroceno é purificado por recristalização a partir de solução em pentano, ciclohexano, benzeno, metanol ou etanol. PERRIN, D.D.; ARMAREGO, W.L.F.; CHAI, C.L.L; “Purification of Laboratory Chemicals.”, Editora Butterworth-Heinemann, Burlington, EUA e Elsivier, Oxford, Inglaterram 5 Ed., Pág. 528 (2009).
Fazem muitos anos que trabalho com o composto. Para recristalizar, experimentei muitos solventes: metanol, etanol, álcool isopropílico, acetato de etila, álcool butílico, hexano, éter de petróleo etc… Durante minha Tese de Doutorado, descobri que cristais maiores e mais bonitos. são obtidos usando tolueno como solvente.
As impurezas do produto comercial, uma olefina usada em sua preparação, o diciclopentadieno, e um pouco de ferro metálico, resultante de decomposição fotoquímica.
Método Clássico. FEDERMAN NETO, A. MILLER, J. (1986) :
Se nunca fez recristalização, consulte o tutorial de recristalização em geral. BAADER, W.J. (2014). Colóquio. Recristalização. Instituto de Química da USP (2014).
Procedimento: Colocar o ferroceno bruto ou de pureza técnica (Usei Aldrich, 97 %), em um erlenmeyer de tamanho adequado, exemplo, 1 litro para 186 g. (1 mol) de ferroceno.
Aquecer tolueno P.A ou de grau técnico, em capela, até a ebulição. Ir adicionando o tolueno fervente, aos poucos, e agitando. Adicione tolueno, agitando, até que todo o sólido sem dissolva. Junte só mais um pouco de tolueno fervente.
Filtre a solução, em funil com papel de filtro pregueado, recolhendo o líquido, o filtrado, e mantendo quente. Remova o aquecimento, deixe esfriar lentamente. Após estar a TA, coloque na geladeira e deixe gelar por 24 horas.
Recolha o sólido precipitado, cristais, purificado, por filtração em papel, ou por filtração a vácuo. Seque o sólido ao ar, ou em um jorro leve de ar comprimido, ou ainda em dessecador sem vácuo.
O ferroceno é útil e mais caro do que o tolueno. Por isso, é preciso recuperar o ferroceno da solução.
A evaporação do filtrado, solvente, ao ar, jorro de ar comprimido, ou evaporador rotatório, fornece uma segunda colheita de cristais, de ferroceno menos puro, que deve ser quardado no frasco de ferroceno recuperado ou bruto.
Recristalização Otimizada e Simplificada de Ferroceno. FEDERMAN NETO, A. (2006):
Ao longo dos anos, modifiquei, otimizei e simplifiquei essa recristalização.
É conhecido que tolueno é bom solvente para recristalizar ferroceno. CORDES, H., BASF, Patente Americana US3217022A (1961-1965), Ref. Chemical Book, mas também é conhecido que é bem solúvel, e forma uma camada de solvatação. TURNER, J.F.C.; SOPER, A.K. Polyhedron, 23, 2975 (2004).
Colocar 186 g. (1 mol) de ferroceno em um frasco erlenmeyer ou balão de fundo chato, de 1 litro.
Adicionar um pouco de tolueno frio, e ferver a mistura, adicionando mais tolueno frio, mas mantendo em ebulição o balão que contem o ferroceno que está sendo dissolvido, Continuar fervendo e juntando tolueno, até que tudo se dissolva. São necessários cerca de 250 ml de tolueno.
Filtre a solução, por papel de filtro pregueado e prossiga como na recristalização clássica.
Características do ferroceno puro:
O Ferroceno é um sólido estável ao ar, considerado pouco tóxico. Ponto de fusão 173-175 ºC. 170-174 ºC, C10H10Fe, mol = 186 g.
O odor do composto bruto é olefínico, lembra um plástico. Mas puro, depois de recristalizado, tem odor agradável, muito semelhante, praticamente igual, ao da cânfora.
Se apresenta como cristais de cor laranja a marrom avermelhado . Quanto maior o cristal, mais escuro. Sublimado recente, são cristais, alaranjados (monoclínicos) , às vezes em agulhas, ou cristais laranja, triclínicos. APPEL, M. Et Al. J. Chem. Phys. 142, 114503 (2015). ESRF (2014). PALIWODA, D. Et Al., J. Phys. Chem. Lett. 4, 4032 (2013).
Recristalizado de tolueno, por nossos procedimentos descritos acima, são cristais marrom avermelhados, relativamente grandes, triclínicos. Preparação por recristalização: FEDERMAN NETO, A. (2022).



Para você ter uma ideia do que é um cristal triclínico, veja sulfato de cobre pentahidratado.
Experimento 2. Provas de Identificação de Ferroceno:
Descomplexação. Presença de Ferro. Primeira prova de Identificação.
FEDERMAN NETO, A. (1986 a 2022).
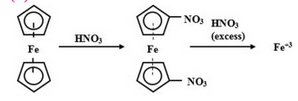
Colocar 2 ou 3 ml de ácido nítrico concentrado, em um tubo de ensaio grande. Em ambiente ventilado e com cuidado, adicionar alguns cristais de ferroceno. Pode ser o reagente comercial. Não precisa ser o recristalizado.
Instantaneamente, ocorre uma vigorosa reação. o ácido nítrico oxida e descomplexa o ferroceno, formando uma solução marrom, com evolução de vapores alaranjados de óxidos de nitrogênio. Dissolva essa solução em água.
Adicione alguns cristais de um tiocianato solúvel. De sódio, potássio ou amônio (fiz com tiocianato de amônio marca Grupo Química).
Forma-se uma coloração vermelha forte do complexo de tiocianato com ferro (III). Indicando a presença de ferro na molécula.
O supõe-se o Ferroceno nitrado, mas nitrocomposto não isolável, e é depois descomplexado, mineralizado. SA, K. Et Al. Mat. Lett. 211, 335 (2018). KNOX, G.R.; PAUSON, P.L. J. Chem. Soc. 628 (1958). Há autores porém, que são de opinião que ferroceno não é nitrável. E sim, ele se oxida a ferricínio e depois descomplexa. HALSTEAD, J.M. Et Al. J. Organomet. Chem. 880, 39 (2019). Mas outros autores reportam que o nitrato de ferricínio é isolável
O resíduo orgânico vindo da degradação completa dos anéis ciclopentadienil, não era estudado até muito recentemente, mas pode, em certas circunstâncias, ser convertido em carbono nanoparticulado, CHALMPES, N. Et Al. (2020). CHALMPES, N. Et Al. Micro 1, 15 (2021).
Reação entre ferro (III) e tiocianato. Que usaremos neste teste. MARTINS, F.G. Et Al. Eclética Química, 30, 63 (2005). A reação, característica, e muito usada em Química analítica (desde 1885), e foi descoberta pelo Químico Sueco Jon Jacob Berzelius em 1826. BERZELIUS, J.J.. WOHLER, F. (Tradutor). “Lehrbuch Der Chemie.” Editora Livraria Arnold, Dresden, Alemanha, Vol 2, Pág. 771 (1826).
Reações que ocorrem, SA, K. Loc. Cit.:
Fe(NO3)3 + 6 NH4SCN = [Fe(SCN)6](NH4)3 + 3 NH4NO3
Essa é uma fácil reação de identificação de ferroceno e mostra a presença de ferro na molécula.
Segunda Prova de Identificação:
Observação: O cátion oxidado do ferroceno, em Inglês, se chama “Ferrocenium“ ou “Ferricenium” ou “Ferricinium“. Em Português, “Ferrocênio“, “Ferrocínio” ou “Ferricínio” Prefiro este último nome, pois se trata do análogo de ferro (III) do ferroceno.

A segunda prova de identificação que faremos, se baseia em uma muito característica reação exclusiva do ferroceno, formação do cátion ferricínio.
Há alguns reportos errôneos, de que ferroceno é estável ao ácido sulfúrico, ROBERTS, J.D.; CASERIO, M.C. “Libre Texts Chemistry. Basic Principles of Organic Chemistry. Metallocenes. (2021). Mas não o é, ele reage com ácidos. Veja BISHNOI, R. , India, Video. “Ferrocene Reaction With Concentrated Sulfuric Acid.” (2020). LITTLE, W.F.; CLARK, A.K. J. Am. Chem. Soc. 25, 1979 (1960).
Ele é primeiro protonado no átomo de ferro, e depois oxidado por ácido sulfúrico, formando um sal de ferricínio, que é o correspondente “Cátion de Ferro (III)” do ferroceno. Descoberta de Wilkinson e cols. (1952). WILKINSON, G.; ROSEMBLUM, M.; WHITING, . M.C.; WOODWORD, R.B. J. Am. Chem. Soc.74, 2125 (1952), . HURVOIS, J.P.; MOINET, C. J. Organomet. Chem. 690, 1829 (2005). TOMA, S.; SEBESTA, R. Synthesis, 47, 1683 (2015). MALICHEWSKI, M. Et Al. Angew. Chem. Int. Ed., 129, 13557 (2017). CHEGG (2022). ERIC, T. Numerade, (2021).
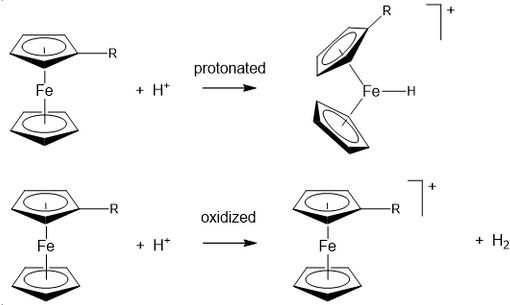
Procedimento. Colocar alguns cristais de ferroceno em um tubo de ensaio. Adicionar 3–6 ml de ácido sulfúrico concentrado. Agitar o tubo ocasionalmente. De início, a solução é verde [Contém ferroceno protonado, ainda ferro (II)], veja a excelente palestra, DOLHUN, J. “MIT Open Course Ware, The Ferrocene Lecture” (2019).
Após cerca de 30-40 min, diluir a mistura com muita água. Forma-se uma bonita solução azul escura por reflexão e vermelha por transparência, dicróica. HUANG, W.H,; JWO, J.J. J. Chin. Chem. Soc. 38, 343 (1991). EVANS, N.H. Et Al. Royal Society od Chemistry, Chemical Science, Londres, Inglaterra (2012).
Observe a forte coloração azul escura, do hidrogenosulfato de ferrícinio. Muito característica. Só ferroceno dá essa reação. FEDERMAN NETO, A. (2022), FEDERMAN NETO, A.; MILLER, J. (1986). SILVA, A.A.S.; FEDERMAN NETO, A. (Orientador) (1994).

2 (C5H5)(C5H5)Fe + 3 H2SO4 = 2 (C5H5)(C5H5)Fe+-HSO4 + SO2 + 2 H2O

Alternativamente, água oxigenada pode ser usada como oxidante.
Assim, ferroceno pode ser rapidamente detectado e identificado por simples testes de tubo de ensaio.
A Química dos sais de ferricínio foi amplamente revisada no excelente artigo: NEUSE, E.W. em: SHEATS, J.E.; CARRAHER Jr., C.E.; PITTMAN Jr., C.U. (Editores), “Metal-Containing Polymeric Systems.” , Springer, Boston EUA e Plenum Press, New York, EUA, Pág. 99 (1983), Reimpressão (1985).
Experimento 3. Acetilferroceno, ou Monoacetilferroceno. e 1,1′-Diacetilferroceno:
O procedimento deste experimento se baseia em uma preparação de rotina para acetilferroceno com alto rendimento ou quantitativa (monoacilação tipo Friedel & Crafts), desenvolvida por mim. DARIN, V.A.; FEDERMAN NETO, A.; MILLER, J.; AFONSO, M.M.F.; FONSATTI, H.C., BORGES, A.D.L J. Prakt. Chem. 341, 588 (1999).
Friedel & Crafts. Clássica reação orgânica dos derivados aromáticos, descoberta pelos Químicos, o Francês Charles Friedel e o Americano James Mason Crafts. FRIEDEL, C.; CRAFTS, J.M. Compt. Rend. Hebdo. Seanc. Acad. Scienc. 84, 1392 (1877). Citado por: Synform, A49 (2018).
Um pós-graduando de nosso Grupo de Pesquisa, Fernando da Costa Archanjo, atualmente Professor da UFVJM. Universidade Federal do Vale do Jequitinhonha e do Mucurí, Diamantina, M.G., descobriu que as quantidades de anidrido acético e de trifluoreto de boro, pode ser muito diminuídas, e a eficiência da reação se mantém. Também ele descobriu que purificar o anidrido acético e o trifluoreto de boro (como fôra feito no método original) não era necessário. FEDERMAN NETO, A.; MILLER, J. ; ANDRADE, V.F.D.; FUJIMOTO, S.Y.; AFONSO, M.M.D.F.; ARCHANJO, F.C. DEL PONTE, G. Zeit. Anorg. Allg. Chem. 638, 209 (2002). ARCHANJO, F.C.; DEL PONTE, G. (Orientador); FEDERMAN NETO, A. (Co-Orientador) (2003).
Trifluoreto de boro gasoso, foi usado como catalisador, para acilar ferroceno, nos anos 50. FISCHER, E.O.; FRITZ. H.P. Adv. Inorg. Chem. Radiochem. 1, 55 (1959). HAUSER, C.R.; LINDSAY, J. Org. Chem.22, 482 (1957). Mas por ser gás, o procedimento é menos prático. Mas o eterato também era ocasionalmente usado. CARTY, P.; DOVE, M.F.A. J. Organomet. Chem. 21, 195 (1970).
Após a publicação do meu procedimento, nos dias atuais, é muito comum usar trifluoreto de boro eterato, BF3.ET2O, como catalisador para acilar ferroceno. Várias Referências. DONAHUE, C.J. ; DONAHUE, C.R. J. Chem. Educ. 90, 1688 (2013).
O método mais usado para acilar ferroceno para fazer acetiferroceno em experimentos de Química é a acilação do ferroceno, catalisada pelo ácido ortofosfórico, descoberta por GRAHAM e cols. GRAHAM, P.J.; LINDSAY, P.V.; PARSHALL, G.W.; PETERSON, M.; WHITMAN, G.M J. Am. Chem. Soc. 79, 3416 (1957).
Sobre esse método, como experimento, veja, há muitos links na Internet. procure por “acetilferroceno” ou ferroceno, acilação“. Um exemplo: DAN, Site Odinity “Investigating the Synthesis and Reactivity of Ferrocene.” (2013).
Há muitos links e videos sobre acetilação de ferroceno catalisada por ácido fosfórico, exemplos, mas há muitos mais. 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78. 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100. 101. 102. 103. 104. 105. 107.
Mas a reação não dá rendimento quantitativo, e frequentemente forma misturas com ferrocenos diacilados e sais de ferrícínio. Por essa razão, neste experimento no Blog, usamos meu método. O eterato de trifluoreto de boro, F3B.(Et)2O, é um catalisador mais conveniente e mais eficiente.
Assim, nosso experimento é diferente da prática de acilação do ferroceno mais conhecida, . Catalisada por ácido fosfórico (ortofosfórico).
Acilação de Ferroceno. Experimento. Acetilferroceno ou Monoacetilferroceno.
O método é excelente e fácil, por isso sugiro seu uso como prática de Química Orgânica ou Inorgânica, em cursos Técnicos de nível médio, ou de Graduação, e mesmo de Pós-Graduação.
Procedimento de FEDERMAN NETO, A. (2022), Modificando procedimentos anteriores de nosso Grupo de Pesquisa. FEDERMAN NETO, A.; ARCHANJO, F.C; DEL PONTE, G. (1999 e 2003). Loc. Cit.
Em um erlenmeyer de 250 ml, colocar 18,6 g (100 mmol) de ferroceno (usei Aldrich) recristalizado. Adicionar excesso, 50-70 ml , de anidrido acético (Merck) e agitar, para suspender.
Adicionar, em pequenas porções, 12 ml (100 mmol) de trifluoreto de boro eterato (Aldrich). A reação é instantânea, a mistura fica vermelha ou violácea. Deixar reagir por 30 min., com agitação ocasional.
Adicionar a mistura sobre gelo, e após o gelo derreter, neutralizar com carbonato de sódio ou bicarbonato de sódio, sólidos, até pH alcalino ao tornassol.
Filtrar o acetilferroceno formado, por papel ou a vácuo, lavar com água e secar ao ar, ou em dessecador sem vácuo.
(Cp)(Cp)Fe + (CH3-C=O)2O = (CH3C=OCp)(Cp)Fe + CH3C=O(OH)

O rendimento varia entre 91 % a quantitativo, (obtido, 92,5 %) e o composto é obtido como sólido laranja escuro. P.F 86 a 89 ºC (geral); Literatura: 85-86. 86-87 ºC, ; HAUSER, C.R.; LINDSAY, J.K. J. Org. Chem. 22, 482 (1957). Li, J.; SU, W.; LIN, J.; CHEN, M.; LI,J. Synth. Comm. 35, 1929 (2005).
Obtido: 87,3 ºC (FEDERMAN NETO, A. (2022). Medido com aparelho de ponto de fusão de capilar Marca Marconi, modelo MA-381, Rampa de aquecimento, 5 graus por minuto.

O produto é suficientemente puro para ser usado como intermediário em Química Organometálica.
1, 1′- Diacetilferroceno:
Resultados novos, nunca publicados antes. FEDERMAN NETO, A. (2022).
Prolongar a reação de acetilação, ou aquecer a mistura a 70 ºC, por uma a duas horas, forma o 1,1′-diacetilferroceno (sólido vermelho), com rendimento moderado a alto (57,3 %), em mistura com sub-produtos resinosos. O derivado organometálico pode ser isolado por dissolução em álcool 95 G.L, tratamento com carvão ativo, filtração e evaporação do solvente em um jorro leve de ar comprimido.


Diacetilferroceno, obtido como um sólido vermelho escuro, P.F. 125,3 ºC, dec.; Medido com aparelho de ponto de fusão de capilar Marca Marconi, modelo MA-381. Lit.: 126-127 ºC. ZHUKOVSKAYA, N.A. Et Al. Russ. J. Gen. Chem. 79, 1660 (2009).
Ao nível do meu conhecimento, diacilação de ferroceno só havia sido conseguida usando cloreto de alumínio anidro ou ácido ortofosfórico , óxido de zinco, como catalisadores.
Trifluoreto de boro catalisava somente monoacilação de ferroceno, a não ser que grande excesso de acilante fosse usado. CARTY, P.. DOVE, M.F.A. J. Organomet. Chem. 21, 195 (1970).
Para diacilação usando trifluoreto de boro, só partindo de ferroceno monoacilado préviamente preparado. MICHNICK, M.J. ; KLEINBERG, J.; McEWEN, W.E. (Orientadores) “Tese de Doutorado em Filosofia, Modalidade Química Orgânica,” Departamento de Química, Universidade d Kansas, Lawrence, Kansas, EUA (1964).
Em contraste com o ferroceno e o monoacetilferroceno, o 1,1′-diacetilferroceno é menos estável e é ligeiramente sensível à luz.
Experimento 4. Como Diferenciar Ferroceno, Monoacetilferroceno e 1,1′-Diacetilferroceno?
É possível diferenciar facilmente pela cor. Ferroceno são cristais amarelo alaranjados ou marrom avermelhados , outro link, (quando em cristais grandes). Acetilferroceno (Monoacetilferroceno) é um sólido laranja escuro, e 1,1′-Diacetilferroceno é um sólido vermelho. , quase cor de vinho. HERTZ, J.E. J. Chem. Educ. 43, 599 (1966).
Outra maneira simples para o Químico efetuar essa diferenciação. A solubilidade em álcool. Diacetilferroceno é mais solúvel em álcool do que Monoacetilferroceno , e este, mais solúvel do que Ferroceno. Veja: ZAKHARENKO, A.V. Et Al. Russ. J. Gen. Chem. 73, 70 (2003). DABROWSKI, M. Et Al. J. Chem. Eng. Data 46, 1627 (2001). ABHAHAM, M.H.; ACREE Jr, W.E. J. Molec. Liquid. 232, 325 (2017). KIM, H.S. Et Al. Electrochem. Comm. 79, 72 (2016). Isso porque diacetilferroceno é o mais polar.
Note as diferenças de solubilidade e cor das respectivas soluções. KUNGFUHL, U. (2018).
Observações sobre a solubilidade de ferroceno e de cetonas ferrocênicas, em água. Oferroceno tem solubilidade negligenciável, em água. Praticamente insolúvel. JI-SHI, W.; KEI, T.; AKIRA, T.; ISAO, S. Bull. Chem. Soc. Japan, 71, 1615 (1998). Em contraste, acetilferroceno e 1,1′-diacetilferroceno, são muito pouco solúveis. ZAKHARENKO, A.V. Et Al. Russ. J. Gen. Chem. 73, 74 (2003). Não localizados em literatura dados sobre a solubilidade de propionilferroceno em água, mas a mim pareceu pouco solúvel, mas mais solúvel do que acetilferroceno.
Experimento 5. Provas de Identificação de Acetilferroceno e 1,1′-Diacetilferroceno.
Acilferrocenos também dão reações colorimétricas.
O “Ensaio do Ferricínio Cátion”, (dissolvendo ferroceno em ácido sulfúrico concentrado) tal com descrevemos no “Experimento 2”, foi repetido, com acetilferroceno e com 1,1′-diacetilferroceno.
Dissolvendo acetilferroceno em ácido sulfúrico concentrado, também se obtem uma solução colorida! Mas ela não é azul, e sim, roxa, violeta, violácea. VOGEL, G.C.; PERRY, W.D. J. Chem. Educ. 68, 607 (1991).
Os sais de acetilferricínio foram descobertos na década de 70, por VAN ZEE. VAN ZEE, J.A.; HALL, D.W. (Orientador), “Substituent Effects Upon the Reactions of Ferrocenes.” Tese de Mestrado, Colorado School of Mines, Golden, Colorado, EUA, Págs. 17, 57, 58 (1972).
Em contraste com o hidrogenosulfato de ferricínio, diluíndo a solução sulfúrica com muita água, o sal de acetilferricínio hidrolisa e a reação reverte para acetilferroceno.
Como no caso do ferroceno sem substituinte, essa oxidação ocorre via uma protonação do acetilferroceno, mas não no átomo de ferro, e sim no carbono carbonílico. Veja NESHVAD, G.; ROBERTS, R.M.G.; SILVER, J. J. Organomet. Chem. 236, 349 (1982).
Repetimos o ensaio, dissolvendo agora o 1,1′-Diacetilferroceno, em ácido sulfúrico concentrado. A solução de hidrogenosulfato de ferricínio correspondente, não é violeta, e sim violeta avermelhada.
Abaixo, formados os hidrogenosulfatos de acetilferricínio (violeta, tubo da esquerda) e 1.1′-diacetilferricínio (violeta avermelhado, tubo da direita) em solução sulfúrica. Foto tirada com câmera digital Kodak Easyshare C-183.

A adição de excesso de água ao conteúdo dos tubos é exotérmica, e regenera as correspondentes ferrocenil cetonas. Mas se os tubos ficarem em repouso, ocorre descomplexação com formação de íons de ferro (III). Prova do tiocionato positiva
Hidrogenosulfato de diacetilferricínio foi reportado, gerado In Situ, em 1972, HORSFIELD, A.; WASSERMANN, A. J. Chem. Soc. Dalton Trans. 187 (1972), e preparado em 1979, e sua descomplexação por sais de cério (IV), estudada. HOLECEK, J.; HANDLIR, K.; KLIKORKA, J. Coll. Czech. Chem. Comm. 44, 1060 (1979). HUAG, W.H.; JWO, J. Chin. Chem. Soc. 343 (1991).
Experimento 6. Complementar. Síntese de Propionilferroceno.
FEDERMAN NETO, A. (2022), substancial modificação do protocolo de DARIN, V.A.; FEDERMAN NETO, A. Et Al., Loc. Cit. (1999).
O Propionilferroceno foi descrito pela primeira vez, em 1957, por HAUSER & LINDSAY, Loc. Cit. Mas uma preparação muito moderna de propionilferroceno foi descrita (após meu artigo de 2009), (em 2014), pela companhia, emprêsa Nanalysis, Calgary, Alberta, Canadá. E por DONAHUE & DONAHUE, Loc. Cit. (2013).
Meu protocolo: 3,7 g (20 mmol) de ferroceno (Aldrich) recristalizado, foi suspenso em excesso (10 ml) de anidrido propiônico comercial (Aldrich, sem purificação prévia). Adicionou-se 3,6 ml (20 mmol) (ou excesso, 4 ml) de trifluoreto de boro eterato.
O ferroceno se dissolve e uma solução púrpura se forma. a mistura foi deixada em T.A, por 15 minutos e depois ligeramente aquecida a cerca de 45-50 ºC, com agitação ocasional, por 2 horas.
A mistura fo jogada sobre gelo. Após o derretimento do gelo, necessário fazer a neutralização. Ocorre que o ácido propiônico que se forma na hidrólise não é totalmente miscível com água, o que mantém o propionilferroceno dissolvido na camada orgânica.
Além disso, propionilferroceno, é um líquido viscoso ou sólido de baixo ponto de fusão (34-39 ºC, DARIN & FEDERMAN NETO Loc. Cit. e HAUSER & LINDSAY, Loc. Cit., e RINEHART Jr., K.L.; CURBY Jr., R.J.; SOKOL, P.E. J. Am. Chem. Soc. 79, 3420 (1957).
Por essa razão, preferí fazer a neutralização com carbonato de potássio anidro, e não com carbonato ou bicarbonato de sódio, para não formar emulsão, neutralizar completamente o ácido propiônico, e melhorar o “Salt Out”, facilitar o isolamento do produto.
Após o gelo derreter, a neutralização foi feita cuidadosamente e pouco a pouco, por adição de várias porções sucessivas de carbonato de potássio anidro, até pH fortemente alcalino (9 a 11, papel indicador universal).
Deixou-se a mistura em repouso em geladeira (§) de um dia para o outro, e o propionilferroceno foi extraído com clorofórmio ou éter (e não com diclorometano, para evitar emulsão). Veja: RAUSCH, M.D.; COLEMAN Jr., L.E. J. Org. Chem. 23, 107 (1958).
Isolamento Alternativo, Procedimento para Laboratórios Pequenos:
Em pequena escala, é possível evitar a extração com solvente. Invés de extrair o propionilferroceno com éter ou clorofórmio… FEDERMAN NETO (2022).
Prepare um funil com papel de fitro, comum, cônico e não pregueado. Gele o funil, o papel e a suspensão com o ferroceno acilado. (§). Filtre. O propionilferroceno é denso, e frio, vai se manter sólido.
Após filtrar, lave o sólido, sobre o filtro, com várias porções de água gelada. Seque ao ar ou em dessecador sem vácuo.
Sólido vermelho vinho, p.f. 37 ºC. Literatura, sólido vermelho escuro, p.f. 38-39 ºC. NESMEYANOV, A.N. Et Al. Bull. Acad. Scienc. SSSR Chem. Scienc. 11, 2142 (1962).
A água vai remover, eluir, quaisquer sais inorgânicos, inclusive o propionato de potássio, que se originou do anidrido propiônico, deixando o ferroceno acilado sobre o filtro. O composto foi secado ao ar.
Os ferrocenos acilados (ferrocenil cetonas) preparados neste artigo não precisam ser recristalizados para serem usados como intermediários químicos.
Mas se quiser recristalizar, muitas referências usam o pentano (36.1) Mas na minha opinião o ponto de ebulição é muito baixo. Sugiro que usem hexano (68,5-69,1) éter de petróleo (60-80), heptano (98,4), ou ciclohexano (80.7).Formam belos cristais coloridos inclusive. Observação: Pontos de ebulição, PE, indicados em Graus Celsius,ºC.
Em minha prática de anos com os ferrocenos, notei que o ciclohexano é excelente, mas para recristalizações de rotina, dos acil ferrocenos, muitas vezes, usei a benzina comum, (50-70) aquela de limpeza, barata – comprar. Benzina Retificada.
O leitor não deve confundir BENZINA com BENZENO. Ainda ocorre essa confusão! A Benzina é uma mistura de alcanos acíclicos (principalmente de 5 a 7 carbonos). Volátil e relativamente pouco tóxica e o organismo a elimina na respiração. Químicamente, é relacionada à gasolina e à aguarrás, removedor, fluido de isqueiro e nafta.
Já o benzeno é um hidrocarboneto aromático cíclico puro, de fórmula C6H6, muito tóxico, cumulativo e cancerígeno.
Além disso, ao contrário do que pensam certos autores, a Benzina não é cancerígena, Link 106, o benzeno sim.
5. OUTROS EXPERIMENTOS, REAÇÕES COM FERROCENOS SUBSTITUÍDOS:
Experimento 7. Reações Tipo Manich, nos sistemas Ferrocênicos.
A Reação de Mannich , Links 108, 109, 110, 111, 112 , 113, 114, 115, 116, 117, 118, é um protocolo geral de Química Orgânica, desenvolvida pelo Químico Alemâo Carl Ulrich Franz Mannich, e seu aluno, Walter Krosche, em 1912. MANNICH, C.; KROSCHE, W. Arch. Pharm. 250, 647 (1912). Uma modificação, foi descrita em 2006. ERKILLA, A.; PIHKO, P.M. 71, 2538 (2006).
É uma condensação entre uma amina primária, ou secundária, ou amônia, e um aldeido não enolisável (como formol) e uma cetona. O produto é bi funcionalizado, uma cetona com grupo amino.
Eu fiz várias reações de Mannich. Ela é limpa e eficiente. SEJER, D., Blog Curly Arrow, Dinamarca (2007). Por essa razão, é muito usada como prática de Química Orgânica, em aulas. MARQUES, M.V.; BISOL, T.B.; SÁ, M.M. Quím. Nova, 35, 1696 (2012).
Neste experimento, iremos fazer uma reação de Mannich, mas organometálica.
As reações tipo Mannich dos sistemas ferrocênicos foram desenvolvidas nos anos 50 e 60. RAUSCH, M.D.; COLEMAN Jr. L.E. J. Org. Chem. 23, 107 (1958). HAUSER, C.R.; PRUETT, L.R.; MASHBURN Jr., T.A. J. Org. Chem. 26, 1800 (1961). LINDSAY, J.K.; HAUSER, C.R. J. Org. Chem. 22, 355(1957). HAUSER, C.; LINDSAY, J.K., LEDNICER, D.; CAIN, C.E. J. Org. Chem. 22, 717 (1957). MASHBURN Jr., T.A.; HAUSER, C.R. (Orientador), “Some Condensations and Related Reactions of Mono and Bis-Acetylferrocenes.” Tese do Doutorado em Filosofia, Departamento de Química, Escola de Artes e Ciências, Universidade de Duke, Durham, Carolina do Norte, EUA (1960). GROESBECK DEWITT III, W.; RINEHART Jr., K.R. (Orientador) “The Coupling Reaction of Ferrocenylmethyl carbonium Ions.” Tese de Doutorado em Filosofia, Modalidade Química, Centro de Graduação da Universidade de Ilinois, Urbana, Illinois, EUA (1966).
6. RESULTADOS, DISCUSSÃO E CONCLUSÃO:
A síntese e purificação do ferroceno, em laboratório, foi revisada e discutida, embora ela seja didática, mas não seja compensadora, do ponto de vista econômico.
A reatividade geral do ferroceno, como um organometálico aromático, também é discutida.
Ferroceno comercial foi purificado por recristalização a partir de tolueno, e identificado por duas reações de tubo de ensaio, simples.
Estes experimentos fáceis foram sugeridos como práticas de Química Orgânica, Inorgânica ou Organometálica, para cursos de nível médio ou superior.
Alguns derivados clássicos do ferroceno, ferrocenil cetonas, foram preparados, acetilferroceno, propionilferroceno e 1,1′-Diacetilferroceno, por acilação tipo Friedel & Crafts modificada, com anidrido acético ou propiônico, catalisada por eterato de trifluoreto de boro, uma rota desenvolvida por meu grupo de pesquisa.
Esse método é vantajoso em relação à outra acilação, muito mais usual, conhecida e geralmente mais usada em experimentos, e catalisada por ácido ortofosfórico.
Uma técnica mais simples para isolar acilferrocenos, que prescinde do uso de extração com solvente, é descrita.
Além disso, ela usa carbonato de potássio, e não os clássicos carbonato de sódio ou bicarbonato. Isso neutraliza totalmente os ácidos acético ou propiônico, e os sais de potássio, não formam emulsão.
Inclusive, em um exemplo, propionilferroceno, que em dias quentes é um líquido viscoso, fica sólido se for resfriado em geladeira, e fica muito mais fácil de ser isolado e estocado.
Ferroceno, acetilferroceno, propionilferroceno e 1,1′-diacetilferroceno, foram oxidados aos correspondentes sais de ferricínio, por ácido sulfúrico concentrado, como base de um novo teste de rotina, rápido, de tubo de ensaio, para identificar os sais de ferricínio, pela cor.
Outro teste simples de tubo de ensaio, mostra a presença de átomo de ferro em ferrocenos e acil ferrocenos, através da descomplexação com ácido nítrico, e posterior reação com tiocianatos solúveis.
O ferroceno sem substituinte e seus derivados acilados (ferrocenil cetonas) foram diferenciados por sua cor, aspecto e solubilidade características.

