
Autoria: Alberto Federman Neto, AFNTECH.
Revisto e Ampliado em 5 de Julho de 2024.
Este artigo trata da História das formas alotrópicas do carbono, e das chamadas “novas” formas alotrópicas do carbono. Na verdade, relativamente novas (desde 1989)!
Também incluindo a grafite (forma alotrópica clássica do carbono), principalmente por sua estrutura e reatividade, e por se material de partida para derivados nanoparticulados de carbono.
1. INTRODUÇÃO:
1.a) Alotropia. Formas Alotrópicas.
É uma característica que alguns elementos químicos tem, de formarem mais de uma (ou várias) substâncias simples, com propriedades organolépticas e físico-químicas diferentes.
Neste Artigo, tratamos especificamente dos alótropos do carbono. Alotropia, Links: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25.
Mas apresentam Alotropia, além do carbono, o enxofre, o fósforo, o silício etc…
2. BREVE HISTÓRIA DA ALOTROPIA E DAS FORMAS ALOTRÓPICAS CLÁSSICAS DO CARBONO:
As formas alotrópicas foram descobertas no elemento enxôfre, (depois estendida ao fósforo) e a Alotropia definida pelo Químico Sueco Jons Jacob Berzelius, (1841).
Como um caso particular de Isomeria (também descoberta de Berzelius), onde o mesmo elemento químico podia formar substâncias simples diferentes. Citações de Berzelius que definem Alotropia:
1. BERZELIUS, J. Unorganische Chemie: Isomerie. (Tradução Livre: Química Inorgânica, Isomeria) Jahres-Bericht 1841, 20, 7–13. Definition on p 13. 2. BERZELIUS, J. Körper Von Gleicher Zusammensetzung und Verschiedenen Eigenschaften. (Tradução Livre: Corpos de Mesma Composição e Propriedades Diferentes.) Jahres-Bericht 1832, 11, 44–48. Definition on p 47. 3. BERZELIUS, J. Isomerie, Unterscheidung von damit analogen Verhältnissen. (Tradução Livre: Isomeria, Distinção entre Condições Análogas) Jahres-Bericht 1834, 12, 63–67. Definition on p 64.
citados por : JENSEN, W.B. J. Chem. Educ. 83 , 838 (2006).
Conhecem-se as clássicas formas alotrópicas do carbono: carbono amorfo (carvão), grafite e diamante. Há muito tempo. Já eram estudadas no séculos XVIII e XIX. PLAYFAIR, L. Proc. Roy. Soc. Edin. 4, 241 (1862).
Variantes de carbono amorfo, são por exemplo, o carvão de churrasco, o negro de fumo, o carvão de hulha, o coque metalúrgico e o carvão ativado, uma invenção de Scheele, popularizada também por Berzelius, Loc. Cit Veja o Item 7, neste Artigo meu.
A existência das diversas formas alotrópicas do carbono já era ideia bem aceita por volta de 1870, conhecendo-se variações de calor específico e condutividade elétrica . HALL, T.W. “New Theory of Galvanism. The Electrothermology of Chemistry.” Editora Edmonston & Douglas, Edinburgo, Escócia, Págs. 22, 24, 53, 54, 63, 84 (1872).
Diamante:
O diamante era suposto, no início, feito do elemento Aristotélico “Terra” puro, “Terra Friável” de Stahl, ou “Terra Vitrificável” de Becher..., como discuti nestes Artigos: 26, 27. LEHMAN, C. (2016).
Incorporando e vibrando por raios de luz, que determinavam a cor do diamante ou da gema STAHL, G.E (Autor); SHAW, P (Tradutor); OSBORN, J; LONGMAN, T. (Editores), “Philosophical Principles of Universal Chemistry.” Pág. 232-237 (1730).
O diamante foi confirmado como formado só pelo elemento químico carbono, pouco antes de 1800. PINKERTON, J. “Petralogy, Treatise on Rocks.” Editora White, Cochrane and Co., Londres, Inglaterra, Vol. 1 , Pág. 542 (1800).
Como havia sido provado pelo Químico Francês Louis-Bernard Guyton de Morveau , analisando e aperfeiçoando experimentos anteriores de Macquer e Lavoisier. tal como citado por KIRWAN, R. (1800). LEHMAN, C. (2016). Diamante é carbono puro. MORVEAU, L.B.G.; TENNANT, M. Annales de Chemie, 25, 72 (1798).
Mas disso discordava o Médico e Químico Suíço Christopher Girtanner. Em seus estudos para diferenciar corpos (hoje substâncias) simples de compostos. Ele achava o diamante muito “cristalino”, para ser carbono… GIRTANNER, C. Phil. Mag. 6, 335 (1800).
Grafite:
E a Grafite, um mineral (natural, mas existe sintético), forma alotrópica de carbono, cristalino em sistema hexagonal…. Seria Carbono puro?
O Farmacêutico e Químico Sueco Carl Wilhelm Scheele foi o primeiro a reconhecer que a grafite era um tipo de carvão. Outro Link. Ele a diferenciou do sulfeto de molibdênio, apesar de ambos os minerais serem lamelares e terem propriedades lubrificantes. MARSHALL, J.L.; MARSHALL, V.R. Hexagonon 8 (2005). ACHESON, J. Franklin Inst. 147, 475 (1899).
A Grafite (substantivo feminino mas às vezes, chamado o grafite), é um mineral, é conhecida a muito tempo. E sabe-se de suas propriedades de conduzir eletricidade. Veja a carta escrita pelo Físico e Químico Italiano Alessandro Giuseppe Antonio Anastasio Volta (descobridor da pilha elétrica) ao Químico Italiano Luigi Brugnatelli . (1794) . Mas Volta supunha que a grafite fosse um metal.
Em que pese sua difícil combustibilidade (grafite é praticamente refratário), se sabia como detectar o elemento carbono na grafite em 1848. ROGERS, R.E., ROGERS, W.B. Am. J. Scienc. Arts 5, 352 (1848).
Mas só no fim do século XIX, através de ataque ácido e posterior combustão, a grafite se torna menos difícil de analisar. SHIMMER, P.W. J. Am. Chem. Soc. 17, 873 (1895).
Por volta de 1860 , o Químico Inglês Benjamin Collins Brodie confirmou que a grafite é sim, composta só por carbono. BRODIE, B.C. Phil. Trans. Roy. Soc. London 149, 249 (1859). BRODIE, B.C. Proc. Roy, Soc. London 10, 11 (1860) . BRODIE, B.C. Quart. J. Chem. Soc. London 12 , 261 (1860).
Em 1872, O Físico e Químico Escocês James Dewar confirmou novamente que a grafite era carbono, através da medida do seu Calor Específico. DEWAR, J. Lond. Edin. Dub. Phil. Mag, J. Scienc. 44, 461 (1872). Dewar se tornaria muito conhecido, por ter sido o inventor da “Garrafa Térmica”.
Grafite ser uma forma alotrópica do carbono foi novamente confirmado, depois por: BOOTH, J.C. J. Am. Chem. Soc. 6, 283 (1884).
No século XX, após os anos 50, mostrar que a grafite é uma forma alotrópica de carbono se torna fácil, usando Espectroscopia Vibracional (Infravermelho, Espectro IR). Vários trabalhos.
Embora a grafite já fosse reconhecida como fibrosa e/ou lamelar ao tempo de BRODIE (Loc. Cit.) COOMÁRA-SWÁMY, A.K. Quart. J. Geol. Soc. 56, 590 (1900). DAWSON, J.W. Quart. J. Geol. Soc. 26 , 112 (1870).
A estrutura mais detalhada da grafite foi estudada a partir dos anos 20, século XX. BERNAL, J.D Proc. Roy. Soc. London A 106, 749 (1924). LIPSON, H.S.; STOKES, A.R. Proc. Roy. Soc. London A 181 , 106 (1942). SLONCZEWSKI, J.C.; WEISS, P.R. Phys. Rev. 109, 272 (1958). HAERING, R.R. Can. J. Phys. 36, 219 (1958).
Na estrutura usual mais moderna, a grafite é composta de lamelas sobrepostas, camadas poliméricas infinitas de anéis hexagonais de carbono sp2 condensados (tipo anéis de benzeno, mas sem hidrogênio).
Cada placa, lamela, é unida a outra, podemos simplificar a ideia, por Forças de Van Der Walls. Mas a intersecção das placas pode ser mais complexa. MATOS, M.J.S.; MAZZONI, M.S.C. (Orientador), Dissertação de Mestrado, UFMG (2009).
TRUCANO, P.; CHEN, R. Nature, 258, 136 (1975). Lab. Cristalografia, UFMG. BELÉM, J. “Recursos Minerais de Minas Gerais. Grafita” . Laboratório de Química de Estado Sólido da UNICAMP (2009). Clube da Química (2022). CROFT, R.C. Quart. Rev. Chem. Soc. 14, 1 (1960). Outro link, confirma a estrutura.
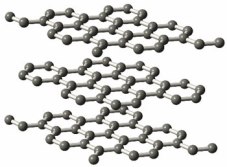
Diferenças entre as estruturas do Diamante e da Grafite. MENTA, E.; MELLO, R.M.; RIBEIRO, M.C. “Portal do Professor, MEC” (2010).
Trataremos agora, das chamadas “novas” formas alotrópicas do carbono. Considerando assim, como alótropos, todas as formas nanoestruturadas de carbono. CHEN, X.; LI, J. Carbon 158 , 1 (2020).
As “novas” formas alotrópicas de carbono, das quais trataremos neste Artigo, são: Fulerenos, Fibras de Carbono, Nanotubos de Carbono e Grafeno. TERRA, A.; MAGALHÂES, A. Rev. Ciênc. Element 11, 33 (2023).
São formas “nanoestruturadas” de carbono. BHATTACHARYA, S. Et Al. Int. J. Nanomed. 9, 1287 (2014). Antigamente chamadas “coloidais”. Contudo, em contraste, “grafite coloidal” é conhecido desde 1936. PORTER, B.H. Rev. Scient. Instrum. 7, 101 (1936).
3. FULERENO. bUCKMINSTERFULERENO:
A imagem que ilustra este artigo representa o Fulereno mais comum, Buckminsterfulereno, uma forma alotrópica relativamente recente (1985) de carbono, de fórmula Molecular Bruta C60.
Imagine uma bola de futebol, formada por 10 anéis aromáticos, tipo os de benzeno, condensados, mas sem hidrogênio. Dessa estrutura (tipo uma bola de futebol), decorre que os fulerenos são ocos por dentro.
Tanto são ocos, que podem reter um átomo metálico em seu interior, como o Lantânio; La@C60. Já não é uma forma alotrópica de carbono, nem substância simples, e sim substância composta, composto.
Descoberto em 1985. HEATH, J.R. Et Al. J. Am. Chem. Soc. 107, 7779 (1985). Excelente revisão: YAMADA, M. Et Al. J. Am. Chem. Soc. 127, 14270 (2005). Fulerenos com lantânio e outros lantanídeos. FLORES, C.M.; BASIUK, V.A. Comput. Theor. Chem. 1217, 113878 (2022).
História dos Fulerenos:
Entre os anos 60 e 70, já haviam alguns trabalhos teóricos que previam que os fulerenos pudessem se formar e que poderiam ser estáveis. JONES, E. New Scientist , 32, 245 (1966). OSAWA, E. Kagaku Kioto Japan, 25, 854 (1970), OSAWA, Kagaku (1970). Trabalhos originais de Osawa não achados, mas citados por KROTO, H. Rev. Mod. Phys. 69, 703 (1997). Veja também em YOSHIDA, M.; OSAWA, E.; AIHARA, J. J. Chem. Soc. Faraday Trans. 91, 1563 (1995).
Excelentes Revisões: KROTO, H.W.; ALLAF, A.W.; BALM, S.P. Chem. Rev. 91, 1213 (1991). MARTÍN, N. Chem. 5, 733 (2019). DE LA FUENTE, F.L.; NIERENGARTEN, J.F. (2012). FOWLER, P.W.; MANOLOPOULOS, D.E. (2006).
Após a descoberta dos fulerenos, o mesmo Osawa (Loc. Cit.), previa Aromaticidade neles. Trataremos disso em outro artigo. OSAWA, E. Phil. Trans. Roy. Soc. A 343, 1 (1993). OSAWA, E. Et Al. “Evolution of the Football Structure for the C60” (2010).
Aromaticidade de Fulerenos. BUHL, M.; HIRSCH, A. Chem. Rev. 101, 1153 (2001). HAIHARA, J.; HOSOYA,H. Bull. Chem. Soc. Japan 61, 2657 (1988).
Cálculos de Aromaticidade tipo dos de Huckel, também previam que fulerenos pudessem existir. BOCHVAR, D.A.; GAL’PERN, E,G. Dokl. Akad. Nauk SSSR 209, 610 (1973).
Também a teórica possibilidade da formação dos fulerenos podia ser calculada matematicamente. ANDREEV, E.M. Matematicheskii Sbornik. Novaya Seriya, 83, 256 (1970).
Mas na prática, não havia ainda nenhum fulereno observado, ou preparado.
Mas estudos de radioastronomia mostravam que cadeias carbônicas insaturadas com duplas ligações podiam se formar no espaço interestelar. SAKATA, A.; NAKAGAWA, N. (1978).
Procurando simular ou reproduzir em laboratório essas condições espaciais, com intuito de investigar formação de compostos orgânicos e as possíveis origens da Vida, três Químicos trabalhavam, o Inglês Harold Walter Kroto, e os Americanos Richard Errett Smalley e Robert Floyd Curl Jr.,
Durante esse trabalho, irradiando grafite com lasers potentes, em 1984 eles observaram e depois isolaram uma molécula nova, composta só de carbono, o fulereno, SMALLEY, R.E. “Great Balls of Carbon.” (1991). BAGOTT, J. (1991).
Tinha a forma de uma bola de futebol, oca por dentro. Modelo de Bola e Bastão:

O trabalho original foi publicado cerca de um ano depois. KROTO, H.W.; HEATH, J.R.; O’BRIEN, S.C.; CURL, R.F.; SMALLEY, R.E Nature 318, 162 (1985). KROTO, H.W.; FISCHER, J.E.; COX, D.E. “The Fullerenes.” Editora Pergamon Press, Oxford, Inglaterra e Ney York, EUA (1993).
Mas pela pequena quantidade produzida ou detectada, alguns Químicos ainda duvidavam de sua existência. ANANTHAIAH, R. , Resonance, 68 (1997). HANDIC, M. Et. Al. Quantum Chemistry 30, 699 (1986).
Mas eu especulo que fulereno pudesse existir antes, mas só não havia sido isolado ou estudado….
Nós químicos, sabemos por experiência própria… Carvão não é solúvel em nada.
Mas por exemplo, no século XIX, o Químico Escocês James Ballatyne Hannay tentava transformar carvão em diamante sintético, e para isso, procurava um solvente para o carvão.
A ideia era solubilizar o carvão e cristalizar diamante por evaporação. Sabemos hoje que isso é impossível, mas durante esse trabalho, Hannay descobriu que carvão era muito, mas muito pouco solúvel em solventes orgânicos! Também ele descobriu os fluidos supercríticos, mas isso é outra História… WISNIAK, J. Rev. CENIC Cienc. Quím. 41, 183 (2010).
Mas tinha uma pequena solubilidade! HANNAY, J.B. Proc. Roy. Soc. London, 31, 200 (1880). HANNAY, J.B. Ibid. 30, 188 (1879). HANNAY, J.B. J. Franklin Inst. 110, 123 (1880).
Em outros experimentos, no início do século XX, o Químico Russo Ivan Ivanovich Ostromislensky , (inventor da borracha sintética), dissolveu um pouco de grafite nos hidrocarbonetos poliaromáticos de alto ponto de ebulição, chamados acenaftaleno e decacicleno. BELTZER, F.J.G. “La chimie industrielle moderne.” Société D’Éditions Techniques. Paris, França, Vol. 1, Pág. 467 (1909). EVEREST, A.E; “The Higher Coal-Tar Hydrocarbons.” Editora Longmans, Green and Company Limited, New York, EUA (1927). Edição Eletrônica, E-Book.
O decacicleno (estrutura) presente em pequena quantidade no alcatrão da hulha foi obtido por síntese orgânica, pela primeira vez, por acoplamento arílico tipo Wurtz-Fittig entre sódio metálico e uma mistura de dibromobenzenos. HOSAEUS, W. Monat. Chem. Werwan. Wissensch. 14, 323 (1893).
Voltando ao assunto fulereno, talvez aquela muito pequena quantidade do carvão ou grafite, que conseguia ser solubilizada, observada por Hannay e por Ostromislensky, fosse fulereno!
Se sabe atualmente que tolueno é um solvente usado para extrair fulerenos das fuligens e de diversos tipos de carvão de arco voltaico. BURLAKOVA, V.E.; NOVIKOVA, A.A. Fuller. Nanot. Carb. Nanost. 25, 483 (2017).
O fulereno foi também detectado no espaço interestelar. MAIER, J.P.; CAMPBELL, E.K. Angew. Chem. Int. Ed. 56, 4920 (2017). Várias referências. E nos Cometas. E em pequeníssima quantidade, na fuligem do carvão ou do diesel queimado e mesmo nas chamas. HOMANN, K.H. Angew. Chem. Int. Ed. 37 , 2432 (1998).
Fulerenos, Obtenção e Usos Tecnológicos:
Pelas moléculas de fulerenos serem interessantes, e terem potencial aplicação tecnológica, tem sido muito estudadas desde sua descoberta.
A síntese do fulereno C60 e de outros fulerenos (Ex. C70) com um número de átomos de carbono maior, foi muito estudada, aperfeiçoada e modificada.
Culminando em dezenas de novos materiais, como fulerenos grandes de muitos átomos de carbono (ex. 240), complexos com átomos de metais coordenados “dentro” da esfera do fulereno e fulerenos substituídos etc…
Em que pese a síntese tenha sido muito melhorada e modernizada, os fulerenos são ainda materiais exóticos e relativamente caros ou muito caros, para o uso em laboratórios simples ou amadores.
Os fulerenos atualmente tem muitas aplicações em Química e em Tecnologia. E podem ser considerados um assunto de pesquisa de ponta.
Pelos muitos usos tecnológicos, estuda-se novas fontes de fulerenos. Por exemplo eles podem ser extraídos da fuligem produzida pelas lâmpadas de arco de carbono, alimentadas por corrente contínua. SEDOV, V.P. Et Al. Russ. J. App. Chem. 93 , 527 (2020). Também da fuligem obtida pela queima de resíduos recicláveis de plástico ou de pneus velhos. FABRY, F.; FULCHERI, L. HAL Open Science (2016).
Pelo desenvolvimento da Química dos Fulerenos, Kroto, Smalley e Curl , dividiriam o Prêmio Nobel de Química de 1996. Veja acima em História dos Fulerenos.
4. FIBRAS DE CARBONO:
Em que pese serem materiais tecnológicos, e não, ao pé da letra, formas alotrópicas de carbono, propriamente ditas, as Fibras de Carbono podem conter anéis de carbono do tipo dos encontrados nos fulerenos. Link 26.
Por isso, as incluo aqui neste Artigo. De fato, há autores que consideram até o negro de fumo uma forma alotrópica do carbono.
História das Fibras de Carbono:
History of Carbon Fiber – A origem é bastante antiga.
Em 1860. O Físico, Químico e Inventor Inglês Joseph Wilson Swan ao fazer um filamento para seu protótipo de lâmpada elétrica, obteve a primeira fibra de carbono.
Os primeiros filamentos de carbono das lâmpadas incandescentes de Edison (veja Item 6, neste Artigo) eram fibras de carbono, embora rudimentares.
As fibras de carbono modernas foram inventadas entre 1960 e 1970, por processos baseados geralmente na carbonização (pirólise) de um filamento orgânico (de plástico, Nylon, poliacrilonitrila, ou de celulose, ou de derivados de petróleo etc..) em atmosfera. inerte (para não queimar). Muitos processos de fabricação, entre 1966 e 1975.
Mas sabe-se, desde 1970, que o melhor precursor para fazer fibras de carbono é a poliacrilonitrila. WILLIAMS, W.S.; STEFFENS, D.A.; BACON, R. J. App. Phys. 41, 4893 (1970). VOHLER, O.; REISER, P.L.; MARTINA, R.; OVERHOFF, D. Angew. Chem. Int. Ed. 9 , 414 (1970). JOHNSON, J.W.; MARJORAM, J.R.; ROSE, P.G Nature, 221 , 357 (1969).
Ao efetuar a pirólise da fibra de poliacrilonitrila em atmosfera inerte, ela carboniza , sem queimar completamente, e forma-se um filamento fino, elástico e resistente, de polímero de carbono, a fibra de carbono.
A sua estrutura é composta por polímeros de anéis hexagonais de carbonos aromáticos sem hidrogênio, como a encontrada na grafite e no grafeno (veremos depois).
5. NANOTUBOS DE CARBONO:
Estruturalmente relacionados à grafite, aos Fulerenos e às fibras de carbono, são os “Nanotubos de Carbono” .
Também considerados entre as novas formas alotrópicas do carbono. SEDERBERG, D. “Allotropes of Carbon.” (2009).
Embora pudessem já existir e talvez tivessem sido observados nas misturas de combustão que formavam fulerenos…
Os “Nanotubos de Carbono” foram observados, isolados e inventados pelo Físico, Microscopista e Inventor Japonês Sumio Iijima, em 1991. IIJIMA, S. Nature 354, 56 (1991).
Ele os observou ao analisar, ao microscópio eletrônico, produtos acumulados no cátodo, de uma vaporização em alto vácuo, de gás inerte argônio, em arco elétrico com eletrodos de grafite ou carvão de retorta, com intuito inicial de obter fulerenos.
Ele os chamou “Microtubos Helicoidais de Grafite“. Hoje chamados “Nanotubos de Carbono“.
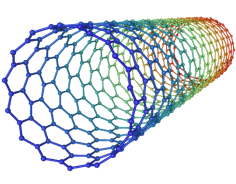
Assim como os Fulerenos, os Nanotubos de Carbono tem um enorme potencial tecnológico, como novos materiais. “Laboratório de Química do Estado Sólido“, Instituto de Química da UNICAMP (2010).
6. GRAFENO:
O Grafeno é uma camada única ultrafina, formada por anéis hexagonais de carbono. Imagine…. é como se fosse uma “única camada” de grafite. Link 27.

História do Grafeno:
SINGH, V. Et Al. Prog. Mat. Scienc. 56, 1178 (2011).
Voltemos ao Item 2 deste Artigo. Grafite.
No século XIX, quando o Químico Inglês Benjamin Collins Brodie Estudava as reações da grafite, e tentou dissolve-la em ácido nítrico e oxidantes, obteve um material que ele achava ser um derivado da grafite, ou uma nova forma alotrópica de carbono que chamou de “ácido carbônico” e depois de “Grafon“. BRODIE, B.C. Quart. J. Chem. Soc. Lond. 12, 261 (1860).
Na realidade, o que ele deve ter obtido é o chamado “Óxido de Grafeno”. Ou o seu polímero multicamadas, o “óxido de grafite”, “óxido grafítico” ou “ácido grafítico”.
Desse material se pode obter o Grafeno (é uma das maneiras). OLIVEIRA, M.; POLLETO, M.; SEVERO, T.C. Rev. Interdi. J. App. Scienc. 3, 16 (2018).
Em 1947, O Físico Teórico Canadense Philip Russel Wallace imaginou a existência das monocamadas de Grafeno, e as usou para calcular a estrutura da grafite. WALLACE, P.R. Phys. Rev. 71, 622 (1947).
Em 1948, foi demonstrada a estrutura lamelar do óxido grafítico. Lamelas que “flutuavam” umas sobre as outras. RUESS, F.V.G.; VOGT, Monat. Chem. 78 , 222 (1948).
Em 1962, através da redução do óxido grafítico, o grupo de pesquisa dos Químicos Alemães Hans Peter Boehm e U Hoffman conseguiram obter uma monocamada de anéis de carbono hexagonais, que viria a ser a estrutura fundamental do grafeno. BOEHM, H.P,; CLAUSS, A.; FISCHER, G.O.; HOFMANN, U. Zeit. Anorg. Allg. Chem. 316, 119 (1962).
Essa monocamada que caracteriza o Grafeno seria confirmada somente cerca de 40 anos depois de 1962. No começo dos anos 2000. Tal como citado (nas refs. 9-12) por: GEIM, A.K. Phys. Script. 014003 (2012).
O nome “Grafeno” foi sugerido para essas estruturas de monocamadas de carbono, por Boehm (Loc. Cit.). BOEHM, H.P.; SETTON, R.; STUMPP, Carbon, 24, 241 (1986).
Em 2004-2005 Os Físicos, o Anglo-Holandês Andre Konstantin Geim e o Anglo-Russo Konstantin Sergeevich Novoselov isolaram as primeiras camadas bidimensionais de Grafeno, através de um engenhoso método…
Aplicando uma fita adesiva, sobre um bloco de grafite sintético pirolítico altamente orientado, e puxando a fita adesiva, nela ficavam aderidas as camadas de Grafeno! NOVOSELOV, K.S.; JIANG, D.; CHEDIN, S.; BOOTH, T.J,; KHOTKEVICH, V.V.; MOROSOV, S.V.; GEIM, A.K. Proc. Natl. Acad. Scienc. 102, 10451 (2005). NOVOSELOV, K.S.; GEIM, A.K. Et Al. Science 306, 666 (2004).
Um método que parece promissor para fazer o grafeno, é pela esfoliação (muito facilitada) da “grafite solúvel” obtida por acilação da grafite com anidrido benzóico, seguida de sulfonação. KELLY, K.F.; BILLUPS, W.E. Acc. Chem. Res. 46, 4 (2013) .
A alguns anos, foi publicada , por pesquisadores brasileiros, uma interessante e prática síntese fácil de derivados de óxido de grafeno, modificados com óxido de ferro, com propriedades magnéticas, e o material de partida é grafite, fácil de encontrar no comércio. Veja meus artigos sobre a História do Magnetismo e materiais magnéticos nanoparticulados, “Ferrofluido“. RHODEN, C.R.B.; AZZOLIN, V.F.; SIQUEIRA, L.; PERINI, M.C.; BULHÕES, L.O.S; MORTARI, S.L. Disciplinarum Scientia, Sér. Nat. Tecnol. 18, 389 (2017) . Outro Link.
Pelo trabalho com o Grafeno e com outros novos materiais mono camada e bidimensionais, Geim e Novoselov receberam o Prêmio Nobel de Física de 2010.
Revisão do Grafeno: LOW, H.S.; NAINAR, M.A.M.; BEGUN, S. Nanomat. Energy 3, 61 (2014).
7. COMPLEMENTOS:
De fato, pelo nível de conhecimento adquirido nos últimos anos, pode-se antever que as “novas” formas alotrópicas do carbono, como os fulerenos, nanotubos e grafeno possam se formar em muito pequenas quantidades, em qualquer combustão de carbono.
Seja uma churrasqueira, como na fuligem, link 28, no negro de fumo na poluição, link 29, das grandes cidades, pela queima dos combustíveis fósseis etc…
Por exemplo, poluição por nanotubos de carbono, foi encontrada no pulmão de crianças moradoras de Paris. Fulerenos podem se formar nas chamas fuliginosas.
Mesmo no carbono amorfo, carvão, podem existir traços de fulerenos e nanotubos. Veja o trabalho de HARRIS, P. Interdis. Scienc. Rev. 24, 301 (2013).
Nesse artigo, o autor cita os estudos de microscopia eletrônica cristalográfica e difração de Raios-X, sobre a estrutura do carvão, do grafite, (além da dupla hélice do DNA) e a estrutura molecular dos vírus, realizado pela Química, Física e Biofísica Inglêsa Rosalind Elsie Franklin.
Ela faleceu prematuramente aos 37 anos, se supõe, vitimada por doenças causadas por excesso de exposição aos Raios-X.
O fato é que “Negro de Carbono”, um tipo de “Negro de Fumo”, foi usado como material de partida para fazer fulerenos e nanotubos. Assim como derivados de petróleo líquidos e gasosos.

