
Autoria: Alberto Federman Neto, AFNTECH.
Revisto e Ampliado em 1 de Agosto de 2024.
Neste Artigo, falaremos sobre o Ferrofluido, uma suspensão coloidal de partículas magnéticas ou magnetizáveis, sensíveis aos imãs e ao campo magnético.
Sua História, preparação, propriedades magnéticas e químicas e uma revisão extensa.
1. COMPOSTOS RELACIONADOS AO FERROFLUIDO:
A Magnetita natural é conhecida a muito tempo, mas o que parece, a primeira menção moderna à existência dos precursores do que muito depois seria o Ferrofluido , suspensão coloidal ou nanopartículas de ferro, ou de óxido de ferro, aparecem como pigmento de óxido de ferro, nos desenhos e quadros do Pintor Norueguês Thomas Fearnley, no início do século XIX. REISSLAND, B.; POULSSON, T.G.; VAN KEULLEN, H.; JOOSTEN, I. Conference: Studying the European Visual Arts, 1850, 82 (2016). HOLTON, E.C. J. Chem. Educ. 5 , 515 (1928).
No final do século XIX, vários Cientistas preparavam, por meios químicos ou elétricos, suspensões ou soluções coloidais de ferro metálico, carbonato férrico, ou de óxidos de ferro. LINEBARGER, C.E. J. Am. Chem. Soc. 20, 375 (1898). REDWOOD, P. Am. J. Pharm. 265 (1880). GRAHAM, T. Phil. Trans. Roy. Soc. London, 151, 183 (1861). GUTHRIE, F. “Practical Physics. Molecular Physics & Sound.” Editora Henry Holte & Company, New York, EUA, Pág. 52 (1879).
Modificações muito mais novas, “Ferro” Coloidal estabilizado com polissacarídeos. HALE, C.W. Nature, 157, 802 (1946). NITO, Y.; STOKES, J.R. Stain Tech. 35, 103 (1960).
Nos dias atuais, se sabe que o ferro coloidal é melhor estabilizado em presença de coloides protetores naturais ou poliméricos. GRIFFITHS, C.H.; HORO, M.P.; SMITH, T.W. J. App. Phys. 50, 7108 (1979). BUTTER, K. Et Al. J. Colloid Interf. Scienc. 287, 485 (2005). OCANA, M,; MORALES, M.P.; CERNA, C.J. J. Colloid Interf. Scienc.212 , 517 (1999). CHOU, K.S.; LEE, S.J. Collo. Surf. A,336, 23 (2009).
Nos anos 80, durante meu extenso trabalho com as reações de compostos organometálicos de ferro, na minha Tese de Doutorado, , links 1, 2, (baixar a Tese, 3, 4), FEDERMAN NETO, A.; MILLER, J. (Orientador) (1980-1986) ……
Notei que soluções coloidais (nanopartículas) contendo ferro metálico e/ou óxidos de ferro, podiam seu obtidas pela decomposição fotoquímica dos organometálicos de ferro, ferropentacarbonilo, Fe(CO)5, e/ou ferro(tetracarbonilo)di(iodeto), Fe(CO)4I2 , ou por simples fotólise da solução neutra ou alcalina, do sal inorgânico nitrato de ferro (III), Fe(NO3)3.
Meus resultados confirmaram observações relacionadas, de outros pesquisadores; Ferrocarbonilo, SMITH, T.W.; WYCHICK, D. J. Phys. Chem. 84, 1621 (1980). Ferro(tetracarbonilo)di(iodeto), POLIAKOFF, M.; TURNER, J.J. J. Chem. Soc. Dalton Trans. 1351 (1973). Nitrato de ferro (III) VAN DER WOUDE, J.H.A. Et Al. Colloid Surf. 8, 55 (1983), Ibid. 8, 79 (1983). Ibid, 12 , 179 (1984). Ibid. 9 , 173 (1984).
O fato é que se sabe hoje, partículas magnéticas coloidais de ferro ou de óxidos mistos de ferro, Magnetita, são um tipo de Ferrofluido. VEREDA, F.; DE VICENTE, J.; HIIDALGO-ALVAREZ, R. J. Colloid Interf. Scienc. 392, 50 (2013). Veja Item 2.
A Magnetita Sintética pode ser obtida de várias maneiras. Link 5. 6. Há vários métodos bons para se fazer nanopartículas de magnetita, que são na prática um ferrofluido, ou a base dele! NICULESCU,A.G.; CHIRCOV, C.; GRUMEZESCU, A.M. Methods, 199, 16 (2022). 7. BLANEY, L. (2017). Exemplo, Magnetita por pirólise seca de gel de óxido de ferro (III), 74, 75,
Embora não tivesse esse nome…. Não havia até os anos 60, nada chamado “Ferrofluido”, ou pelo menos, assim não era chamado.
Datam de 1915-1917 as primeira tentativas de se fazer óxidos magnéticos de ferro sintéticos. SOSMANN & ROSTETTER , Artigos entre (1914-1917). Entre 1922 e 1928, a Magnetita sintética (por queima de ferro) era preparada e usada como catalisador em síntese orgânica. RAAL, F.A. S. Afric. J. Chem. 8, 90 (1925). HERROUN, E.F.; WILSON, E. Proc. Phys. Soc. 41, 100 (1928). WYCKOFF, R.W.G.; CRITTENDEN, E.D. J. Am. Chem. Soc. 47 , 2866 (1925).
Um dos métodos usuais modernos para fazer Magnetita sintética, é a co-precipitação de cloretos ferroso e férrico por amônia. MARTINEZ-MERA, I., Et Al. Mat. Lett. 61, 4447 (2007).
Esse processo de co-precipitação de ferro (II) e (III) (usando sais ferrosos e férricos) em meio alcalino, é hoje muito usado, e é o principal protocolo para preparar Magnetita sintética.
Ele foi desenvolvido em 1925-1933, WELO, L.A.; BAUDISCH, O. Lond. Edin. Dub. Phil. Mag. J. Scienc. 50, 399 (1925). BAUDISCH, O.; WELO, L.A. Naturswisschaften, 21, 659 (1933). Ibid. 593 (1933) e utilizado para obter Magnetita a partir do líquido proveniente do ataque ácido de meteoritos de ferro. SPIROFF, K. Econ. Geol. 33, 818 (1938). Excelentes Revisões, “Reviews”, WELO, L.A.; BAUDISCH, O. Chem. Rev. 15, 45 (1934). Ibid., 15 , 1 (1934). Reação descoberta pelo Químico, Fotoquímico e Bioquímico Austríaco Oskar Baudisch e seu Assistente, Lars Alvin Welo.
2 FeCl3 + FeCl2 + 4 H20 + 8 NH3 = Fe3O4 + 8 NH4Cl
ORTIZ, N.; BRESSIANI, J.C. (Orientador), Tese de Doutorado em Ciências, Área de Tecnologia Nuclear, Instituto de Pesquisas Energéticas e Nucleares, Universidade de São Paulo, USP (2000). BALEK, V. ; SUBRT, J; Pure Applied. Chem. 67, 1839 (1995). Links 7 , 8 , 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. WELO, L.A, BAUDISH, Chem. Rev. 15, 45 (1934).
Nas etapas iniciais, hidróxidos de ferro (II), Fe(OH)2 e Ferro (III), Fe(OH)3, (ou modernamente , FeO(OH)·H2O) se formam e desidratam espontaneamente. “Reação de Schikorr“ , SCHIKORR, G. Zeit. Elekr. Angew. Physik. Chem. 35, 65 (1929). Do Químico Alemão Gerhard Oskar Emil Schikorr .
A Fórmula “moderna”, FeO(OH).H2O para o hidróxido de ferro (III), antigamente Fe(OH)3 (como ainda é clássico nos livros) parece ser a correta, como demonstrado pelo Famoso e Brilhante Químico Analítico Holandês Izaak Maurits Kolthoff . KOLTHOFF, I.M.; MOSKOVITZ, B. J. Am. Chem. Soc. 58, 777 (1936).
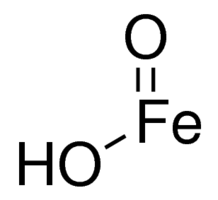
Além de ser preparada, a Magnetita também pode ser comprada em pó,
Veremos depois, Item 2, que essa Magnetita artificial, tem tudo a ver com Ferrofluido. 19.
2. FERROFLUIDO. DESCOBERTA e HISTÓRIA:
Vimos, no Item 1 que existiam métodos para preparar suspensões de Magnetita artificial… Mas não havia Ferrofluido, ainda, até os anos 60.
Ferrofluido é uma solução ou suspensão coloidal (nanoparticulada) de Magnetita Artificial suspensa em óleo, água, ou um solvente, e em presença de um surfactante. Link 19.
É sensível aos imãs e suas partículas se aglomeram formando figuras geométricas e espículos, pois cada partícula se comporta como se fosse um minúsculo imã, polarizada pela aplicação de um campo magnético externo….

Veja também:
HAPP, R.S.L.; LUNAZI, J.J (Coordenador); HAPP, J.F. (Orientador); COELHO, A.A (Coorientador) Relatório Final, Tópicos de Ensino de Física, Instituto de Física, Universidade de Campinas, UNICAMP (2010). LIAO, W.H.; KRUEGER, D.A. J. Colloid Interf. Scienc. 70, 564 (1979). MITSUMATA, T. Et Al. J. App. Phys. 85, 8451 (1999). KARASINSKI, V. TecMundo, (2012). ROSA, A.P.; CUNHA, F.R. (Orientador), “Microestrutura e Magneto-Reologia de Ferrofluidos em Cisalhamento : Teoria e Simulação.” Tese de Doutorado em Ciências Macânicas. Universidade de Brasília, Brasília, D.F. (2018).
O Ferrofluido foi inventado em 1962-1963, pelo Engenheiro Mecânico e Cientista da NASA, Solomon Stephen Papell, “Steve Papell”. PAPELL, S.S. Patente Americana, US3215572A (1963-1965). SCHERER, C,; FIGUEIREDO NETO, A.M. Braz. J. Phys. 35, 718 (2005).
Pela mesma época, foi pesquisada na Bélgica, uma formulação semelhante. NEURINGER, J.L.; ROSENSWEIG, R.E. Phys. Fluids, 7, 1927 (1964). O’CONNOR, T.L. Patente Belga, Diamond Alkali Co. (1961-1962).
Na tentativa de obter um combustível de foguete que pudesse ser levado para o tanque por um campo magnético. A ideia era poder bombear fluidos em Gravidade Zero. Papell imaginou que um imã carregaria o fluido, e as partículas metálicas, por serem mais densas, decantariam e não seriam levadas para o tanque.
Por conter metais não combustíveis e impurezas, nunca pode ser usado para isso. ARRIGHI, R.S. NASA (2021).
Mas Ferrofluido tem propriedades interessantes e vários usos tecnológicos, experimentais e até recreativos. Por isso, foi muito modificado, aperfeiçoado e modernizado. 73, ZAHN, M.; SHENTON, K. IEEE Trans. Magn. 16, 387 (1980). Diversos Artigos e Patentes.
Pelas importantes aplicações, até nos dias atuais, existem muitas variantes de Ferrofluido sendo inventadas, pesquisadas e desenvolvidas. KOLE, M.; KHANDEKAR, S. J. Magn. Mag. Mat. 537, 168222 (2021). OEHLSEN, O. Et Al. ACS Omega, 7, 3134 (2022). WANG, W. Et Al. J. Nanopart. Res. 24, 102 (2022). PHILIP, J. Adv. Colloid Interf. Scienc. 311, 102810 (2023).
3. PREPARAÇÃO DO FERROFLUIDO:
Pode-se comprar o Ferrofluido no Brasil, embora não seja tão barato. Links: 20, 21, 22, 23, 24, 25, 26.
Mas existem várias maneiras de prepará-lo. Compare com o Item 2, e verá que há correlação, pois o Ferrofluido são partículas de Magnetita.
Revisões dos métodos de obtenção de Ferrofluido. JAIN. N. Et Al. ACS App. Mat. Interf. 3, 662 (2011). OEHELSEN, O. Et Al. ACS Omega, 7, 3134 (2022). GENC, S.; DERIN, B. Curr. Opin. Chem. Eng. 3, 118 (2014). VÁRIOS AUTORES; ODENBACH, S. (Edtor), “Colloidal Magnetic Fluids.” Editora Springer, Dresden, Alemanha (2009). BACRI, J.C.; MASSART, R. Et Al. J. Magnet. Mag. Mat. 85, 27 (1990). DHUMAL, J. Et Al. Int. J. Mat. Chem. Phys. 1, 141 (2015). SANTOS, E.; ALBO, J.; IRABIEN, A. RSC Adv. 4, 40008 (2014).
Destacaremos alguns métodos mais simples para preparar Ferrofluido.
Um método usual, é fazer a neutralização de uma solução contendo cloreto de ferro (II) e cloreto de ferro (III), com amônia aquosa, que é o amoníaco (antigo hidróxido de amônio). 70, Em óleo, isoparafina, ou outro solvente (geralmente querosene), e adicionando um surfactante , (geralmente ácido oléico ) 27, 28, 29, 30, 31, 32, 33, 34, 35. 36. 37. 38. 39. 40. 41. 42. 43. 45. 46. Hidróxido de tetrabutilamônio, 72. Pode até ser feito em água. BERGER, P. Et Al. J. Chem. Educ. 76, 943 (1999) ou água e sal. Veja também: VASCONCELOS, V.C.M.; LENZ E SILVA, V.S.B. (Orientador) “Sintese de Nanopartículas de Óxido de Ferro…..” Trabalho de Conclusão de Curso Para Obtenção do Grau de Engenheiro de Materiais, Escola Politécnica da Universidade de São Paulo, São Paulo, S.P. (2019).
De maneira análoga ao que vimos no Item 1, veja também detalhes da preparação e como funciona o Ferrofluido , em: BIOHAZARD, Blog Química em Ação! (2009).
2 FeCl3 + FeCl2 + 8 NH3 + 4H2O –> Fe3O4 + 8 NH4Cl
Hidróxido de Sódio também pode funcionar, , 77, mas o excesso de sais de sódio pode ser difícil de eliminar. Usar amônia misturada com de hidróxido de sódio, é o processo moderno otimizado de Massart. Co-precipitação de cloretos de ferro (II) e (III), por amoníaco (amônia aquosa, antigo chamado hidróxido de amônio) e hidróxido de sódio. MASSART, R. IEEE Trans. Magnet. 17, 1247 (1981). 81. BEE, A.; MASSART, R.; NEVEU, S. J. Magnet. Mag. Mat. 6, 149 (1995). Ou hidróxido de sódio sozinho. procedimento otimizado de LOKHAT, D.; OLIVER, M.; CARSKY, M. Pol. J. Chem Tech. 17, 43 (2015).
O cloreto de ferro (II) pode ser comprado, ou feito de ferro metálico e ácido clorídrico, , 45, ou pelo meu método, reduzindo solução aquosa de cloreto de ferro (III) (ou percloreto de ferro para eletrônica), 72, com ferro metal, pregos ou Esponja de aço. Veja uma variante, em 45. 46.
Há trabalhos aonde a co-precipitação é feita já na presença de um campo magnético. O que facilita o processo. HONG, R.Y. Et Al. J. Magnet. Mag. Mat. 310, 37 (2007).
Para fazer Ferrofluido, uma simplificação do método acima, é partir só de cloreto de ferro (III) e efetuar sua redução no meio da neutralização. por exemplo, parte do ferro (III) é reduzido com álcool. ou com ferro. 41. 44. 45. 46. 51
Ou preparar o óxido magnético por pirólise do cloreto de ferro (III). 49. Ou oxidar com água oxigenada , parte do cloreto de Ferro (II) preparado de pregos ou parafusos e ácido clorídrico. 68. Pode-se ainda usar cloreto de ferro (III) e sulfato de ferro (II).
Ou ainda de sulfato de ferro (II) , hidróxido de sódio e nitrato de potássio em presença de ar, como oxidante para formar Ferro (III). Similar com hidróxido de potássio. 82, Ou usar diversos sais de ferro (II) e ferro (III). Pirólise de acetato de ferro (III). Ou cloreto de ferro (II), nitrato de ferro (III) e nitrato de sódio como oxidante. Cloreto de ferro (III), amoníaco e sulfito de sódio como redutor. Sulfato de ferro (II), cloreto de ferro (III) e hidróxido de sódio, COLTRO, M.C.R.C. Et Al. Lat. Am. J. Devel. Curitiba, 3, 2738 (2021).
Há outro método bom e rápido, a partir de cloreto de ferro (III) em álcool, mas o redutor usado (cloridrato de fenilalanina metil éster) não é fácil de se encontrar no comércio. PARNICA, J.; KESA, P.; KOVAC, J.; TIMKO, M.; ANTALIK, M. Acta Phys. Polon. A, 126, 276 (2014).
Procedimento bom e detalhado. Para fazer Ferrofluido por co-precipitação. Outro método otimizado, Outro método.
Há métodos mais simples descritos. Por exemplo suspender direto óxido preto de ferro comercial. 47, 48, 50. Revisão dos métodos de obtenção.
Um método mais complicado e não acessível sem equipamento especial, seria reagir (oxidar) o ferro metálico com vapor de água. GOTO, T.G.; MOREIRA, J.R.S. (Orientador), “Estudo Experimental do Processo de Oxidação do Ferro com Vapor De Água, Para Produção de Gás Hidrogênio.” Dissertação de Mestrado em Ciências, Área de Concentração Engenharia Mecânica de Energia e Fluidos, Escola Politécnica da Universidade de São Paulo (2016).
Tenho em mente, mas ainda não pude testar, que se possa usar Magnetita em Pó Fino comercial, 67. 75, De fato, eis fluidos magnéticos feitos com Magnetita. 76, 77, 78, 79, 80
Ou mesmo pó de ferro fino. Porém feito com ferro em pó, não será um Ferrofluido verdadeiro, visto que pó de ferro não é uma imã, não é um pó magnetizado, mas experimentos interessantes podem ser feitos. 51, 52, 53, 54. 66.
Outros Autores usaram pó de ferro com pó de neodímio. Interessante mas caro. Mundo de Bob (2021).
Não é Ferrofluido clássico, mas pode ser usado para fazer suspensões coloidais magnéticas…
A alguns anos, foi publicada , por pesquisadores brasileiros, uma interessante e prática síntese fácil de derivados de óxido de grafeno, modificados com óxido de ferro, com propriedades magnéticas, e o material de partida é grafite, fácil de encontrar no comércio. Veja meus artigos sobre a História do Magnetismo e as Formas Alotrópicas do Carbono. RHODEN, C.R.B.; AZZOLIN, V.F.; SIQUEIRA, L.; PERINI, M.C.; BULHÕES, L.O.S; MORTARI, S.L. Disciplinarum Scientia, Sér. Nat. Tecnol. 18, 389 (2017) . Outro Link.
Mais um método simples e recente, para fazer nanopartículas magnéticas de óxidos de ferro. O material de partida é cloreto de ferro (III), e parte do ferro é reduzido a (II), usando sulfito de sódio como redutor. amônia aquosa é o álcali… LAVAYEN, V.; NATIVIDADE, L.A. Et Al. RSE J. Res. Soc. Dev. 10, e27310817184 (2021). Outro Link.
4. FERROFLUIDO CASEIRO E FÁCIL:
Há uma outra maneira bem simples de obter Ferrofluido, mesmo sem laboratório. Uma interessante maneira caseira.
Ela se baseia na queima, combustão de “lã de aço“, Esponja de aço, tipo o popular “Bombril“.
Vocês sabem, esponja de aço, lã de aço, é aquela esponja metálica de cozinha, para lavar panelas. Ela é composta de finos filamentos de ferro metálico , CHEMELLO, E. (2010), ou de aço de baixo carbono. PEREIRA, E.S. Et Al. (2013).
O processo caseiro de fazer Ferrofluido, se inicia com a queima da lã de aço. Coloque-a em um recipiente adequado (panela, refratário ou cápsula de porcelana grande) e acenda-a com um fósforo, isqueiro ou um maçarico.
Essa queima irá transformar o ferro, em óxido magnético de ferro, óxido misto de ferro, Magnetita:
3 Fe + 2 O2 = Fe3O4
Importante destacar que você não deve “agitar” nem “soprar” a palha de aço queimando, não só por causa das fagulhas, mas também porque a alta temperatura produzida e a quantidade maior de oxigênio, iriam provocar a oxidação completa do ferro, o que não é desejável, pois formaria o óxido de ferro (III), que não é Magnetita, não é um material magnético.
4 Fe + 3 O2 = 2 Fe2O3
Resumo, não queremos fogos de artifício, queremos Magnetita! Precisamos de combustão incompleta. Mas em certas condições, usando muita lã de aço, FeO, óxido de ferro (II) pode ser formado.
Links para esse processo de preparar Magnetita. 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65.73.
Uma Dica minha, de Químico. tem de ficar preto ou cinza escuro. qualquer coloração puxando para o marrom, indica formação de óxido de ferro (III), Fe2O3. Um material não magnético.
Para formar Ferrofluido, essa Magnetita preparada da lã de aço, vai ser triturada ou peneirada, vai ser incorporada exemplo em óleo comestível, 60, 62, 63, óleo mineral, 67 , óleo lubrificante de motor, 69. As vezes um solvente, como querosene, ciclohexano, e um surfactante, ácido oleico, 67. linoleico, ácido palmítico, ácidos graxos de 14 ou 18 carbonos, sabão em pó, 63 , sabão comum. 68. detergente. Mesmo ácido cítrico.

